FDA批准对一种形式Batten病的第一个治疗。
在FDA的药品评价和研究中心中药物评价III办公室主任Julie Beitz,M.D.说:“FDA承诺为有罕见病患者批准新和创新治疗,尤其是那里没有被批准的治疗选择,” “批准第一个为Batten病的这个形式治疗是对患这种情况患者是一个重要进展。”
优先审评和突破性治疗指定。孤儿药物指定,罕见儿童疾病优先审评凭证。
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/761052lbl.pdf
处方资料重点
这些重点不包括安全和有效使用BRINEURA需所有资料。请参阅BRINEURA完整处方资料。
BRINEURA(cerliponase alfa)注射液,为静脉使用
美国初次批准:2017
适应证和用途
Brineura是一种水解溶酶体N-端三肽氨基肽酶适用于在3岁和以上有婴儿晚期神经元蜡样脂褐质沉积症2型(CLN2)症状性儿童患者减慢步行的丧失,也被称为三肽氨基肽酶1(TPP1)缺乏。(1)
剂量和给药方法
● 无菌术:制备和给药期间必须严格地观察。Brineura应由在脑室给药中知识渊博的医生给药,或或在他的指导下给药。Brineura是通过输注经过一个外科地植入的贮存池和导管给予至脑脊液(CSF)。(2.1)
● 建议在输注开始前30至60分钟用抗组织胺类有或无解热药或皮质激素预先-治疗患者。(2.2)
● 推荐剂量是300 mg每间隔一周给药一次作为一个脑室内输注接着通过脑室内输注电解质 历时约4.5小时。(2.2)
●对关于制备,特异性脑室内接入装置使用,和给药的完整资料,见完整处方资料(2.1,2.3,2.4,2.5)
剂型和规格
注射液:Brineura 150 mg/5 mL(30 mg/mL)溶液,每纸盒两个单次-剂量小瓶与脑室内电解质注射液5 mL在一个单次-剂量小瓶共包装。(3)
禁忌证
● 急性脑室内接入装置-相关并发症(如,渗漏,装置失效,或装置-相关感染)。(4)
●用脑室-腹膜分流术患者。(4)
警告和注意事项
●脑室内接入装置-相关并发症:检查头皮皮肤完整性和脑室内接入装置渗漏的迹象。如存在装置渗漏或感染的征象不要给药。
常规地输送CSF样品为测试检测亚临床装置相关感染。(2.5,5.1)
● 心血管不良反应:输注前,期间,和输注后监视生命征象。在有心动过缓,传导疾患,或有结构性心脏病病史患者,在输注期间监视心电图(ECG)。在无心脏异常患者,每6个月进行常规12-导联ECG评价。(2.5,5.2)
● 超敏性反应:输注期间和后观察患者。如发生一个严重的超敏性反应,立即地停止输注和开始适当的治疗。(5.3)
不良反应
最常见不良反应(≥8%)是:发热,ECG异常,减低CSF蛋白,呕吐,癫痫,超敏性,增加CSF蛋白,血肿,头痛,易激惹,脑脊液细胞增多,装置-相关感染,心动过缓,感觉不舒服,和低血压。(6.1
完整处方资料
1 适应证和用途
Brineura是适用为3岁和以上有在症状性儿童患者有婴儿晚期神经元蜡样脂褐质沉积症2型(CLN2),也被称为三肽氨基肽酶1(TPP1)缺乏减慢步行的丧失。
2 剂量和给药方法
2.1 重要制备和给药资料
● 制备和给药期间无菌术必须被严格地观察。
● Brineura应被脑室内给药知识渊博的医生,或由他指导下给药。.
● Brineura是通过输注给予至脑脊液(CSF)通过一个外科植入的贮存池和导管(脑室内接入装置)。Brineura是意向通过Codman® HOLTER RICKHAM贮存池(部件号:82-1625,82-1621,82-1616)与Codman®脑室导管(部件号:82-1650)给药。首次输注前脑室内接入装置必须被植入。建议首次剂量被给予至少在装置植入后5至7天。
● Brineura是意向用B Braun Perfusor®空间输注泵系统给予。
对用于输注Brineura的这个注射器泵系统的基本性能要求如下:
o 输注速率为2.5 mL/hr与输注准确度为+/- 1 mL/hr
o 兼容性 与提供的为与Brineura使用在给药盒内20 mL注射器。
o 阻塞警报设置至 ≤ 281 mm Hg
● 利用在给药盒提供的与Brineura组分使用给予Brineura和脑室内电解质[见如何供应/贮存和处置(16)].
2.2 剂量
在儿童患者3岁和以上Brineura的推荐剂量是通过脑室内输注给予300 mg每隔一周一次。首先给予Brineura接着通过输注脑室内电解质每次在一个输注速率2.5 mL/hr。Brineura输注的完成,包括被要求输注的脑室内电解质,是大约4.5小时。
建议在输注开始前30至60分钟患者用抗组织胺类 有或无解热药或皮质激素的预先-治疗。
2.3 给药的方法
必须仅脑室内途径给予Brineura和脑室内电解质,利用提供为Brineura使用的的给药药盒。Brineura和脑室内电解质每个小瓶仅为单次剂量使用。
每次输注10 mL Brineura的组成接着2 mL的脑室内电解质。必须利用一个输注组件有一个0.2 µm在线滤器给药完成输注。为了完全地给予Brineura使用脑室内电解质冲洗输注线,端口针,和脑室内接入装置和维持脑室内接入装置效力。
2.4 对输注的制备
收集用品:
● Brineura和脑室内电解质注射液小瓶(2个的包装1)[见如何供应/贮存和处置(16)]
● 为用Brineura使用给药药盒(2个的包装2 )[见如何供应/贮存和处置(16)]
● 注射器泵(不提供)
检查给药药盒输注组分确保在组分是在各个包装内和没有损坏。
在室温解冻Brineura和脑室内电解质注射液小瓶共约60分钟。不要用任何其他方法解冻或加温小瓶。不要摇晃小瓶。解冻阶段期间将发生凝聚。不要再次-冻结小瓶或冻结含Brineura或脑室内电解质的注射器。
检查完全地已解冻的Brineura和脑室内电解质注射液小瓶。肠道外药品每当溶液和容器许可,在给药前应视力检查颗粒物质和变色。Brineura是一种清晰的微乳白色和无色至浅黄色溶液。脑室内电解质是一种清晰至无色溶液。如溶液是变色或如在溶液中存在其他外来颗粒物质不要使用。Brineura小瓶可能偶然含西半透明纤维或不透明颗粒。这些自然存在颗粒是cerliponase alfa。
这些颗粒通过0.2 mµ在线过滤器被去除对Brineura的纯度和强度没有可检测到影响。脑室内电解质可能含颗粒,它出现在解冻阶段期间;但是,这些当溶液达到室温溶解。
2.5 脑室内输注操作
Brineura的脑室内输注 图1代表一设立的脑室内输注系统。输注期间使用无菌术。遵循以下步骤进行用脑室内输注。
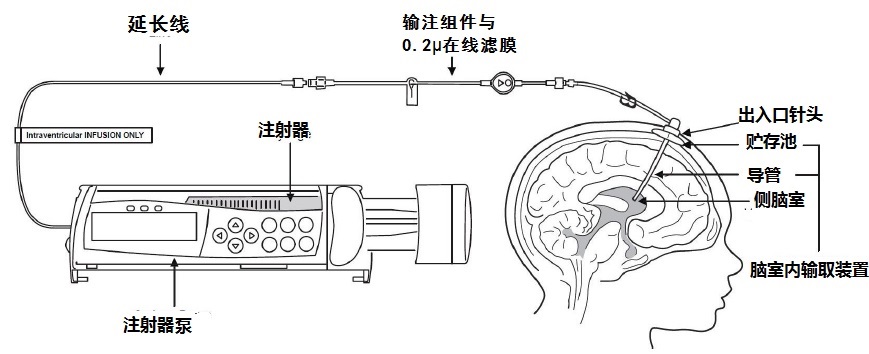
图1
1. 使用无菌术当为输注准备Brineura注射器。标记一个无菌注射器为“Brineura”和附着注射器针头。从两个Brineura小瓶取下绿色可翻盖[flip-off caps]。用标记“Brineura” 注射器抽吸总量 10 mL。
不要稀释Brineura。Brineura不要与任何其他药物混合。
2. 标记输注线 “仅为脑室内输注”(见图1)。
3. 附着标记注射器含Brineura至延伸线(见图2)。然后连接延伸线至有一个0.2 mµ在线滤膜的输注组件(见图1)。

4. 用Brineura灌注输液组件。
5. 检查头皮对脑室内接入装置渗漏或失效和对潜在感染的征象[见警告和注意事项(5.1)]。
6. 为脑室内输注每次标准医护开始准备头皮。
7. 端口针插入至脑室内接入装置(见图3)。
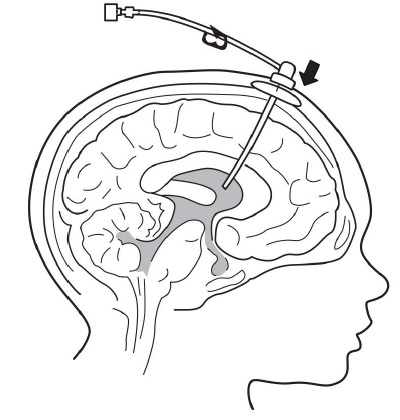
8. 连接一个分开的空的无菌一次性-使用 luer lock注射器,不大于3 mL(不提供)至端口针. 抽吸0.5 mL至1 mL的CSF核查脑室内接入装置的效力(见图4)和送标本为培养。
● CSF不要返回至脑室内接入装置。
● 为感染监视常规地送CSF样品 [见警告和注意事项(5.1)]。
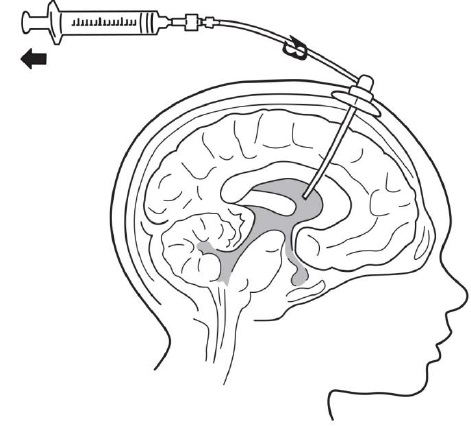
9. 附着输注设置用0.2 mµ在线滤膜至端口针(见图1)。
●每次标准医护开始固定组件。
10. 放置含Brineura注射器至注射器泵和程序泵输送在一个输注率为2.5 mL每小时。设置阻塞警报设置在压力 ≤ 281 mm Hg警报。详细见注射器操作手册。不要作为一个推着或手工地输送。.
11. 输注开始前30 至60 分钟预先给药[见剂量和给药方法(2.2)]。
12. 输注开始前,输注期间,和输注后定期地监视生命征象(血压,心率) [见警告和注意事项(5.2)]。
13. Brineura的初始输注在一个输注2.5 mL每小时。
14.输注期间定期检查输注系统对渗漏征象或输注失败[见警告和注意事项(5.1)]。
15. 当Brineura 输注完成,从泵脱开和取下空注射器和从管解开连接(见图5)。对脑室内电解质输注进行14步骤。
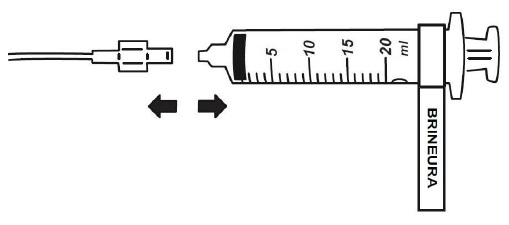
脑室内电解质的脑室内输注
Brineura输注被完成后给予提供的脑室内电解。
16. 用无菌术当为输注准备脑室内电解质注射器。标记一个无菌注射器为“脑室内电解质”和附着注射器针头。从脑室内电解质注射液小瓶取下黄色翻转帽。抽吸2 mL的脑室内电解质。遗弃留下的未使用部分。
17. 附着注射器至延伸线。(见图6).
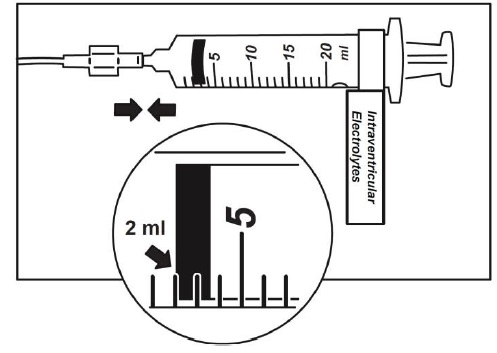
18. 放置注射器含脑室内电解质入注射器泵和程序泵以输送在一个输注率2.5 mL每小时。设置阻塞警报设置在压力≤ 281 mm Hg警戒。详见注射器操作手册。不要作为一个推注或手工地输送。.
19. 脑室内电解质的起始输注在一个速率2.5 mL每小时。
20.输注期间定期地检查输注对渗漏的征象或输送失效.
21. 当脑室内电解质输注完成,从泵脱附着和取下空注射器和从输注线解开连接。
22. 取下端口针。每次标准医护输注部位加以轻压力和绷带。
按照当地要求遗弃输注组分,针头,未使用溶液和其他废料。
已解冻的产品的贮存
立即地使用已解冻的Brineura和脑室内电解质。如不立即地使用,贮存未打开的小瓶在冰箱在 2°C至8°C和在24小时内使用。.
在注射器中产品的贮存
立即地使用有标记的注射器。如不立即地使用,贮存有标记注射器在冰箱内在2°C至8°C直至输注前 4小时。
3 剂型和规格
注射液:Brineura 150 mg/5 mL(30 mg/mL)溶液,每纸盒两个单次-剂量小瓶与脑室内电解质注射液5 mL在一个单次-剂量小瓶共包装。乳白色和无色至浅黄色溶液。脑室内电解质是一种清晰至无色溶液[见如何供应/贮存和处置(16)]。
4 禁忌证
以下患者禁忌用Brineura:
● 急性脑室内接入装置-相关并发症(如,渗漏,装置失效,或装置相关感染)[见警告和注意事项(5.1)]。
●脑室-腹膜分流术.
5 警告和注意事项
5.1脑室内接入装置-相关并发症
Brineura必须用无菌术给予以减少感染的风险。每次输注前卫生保健专业人员应检查头皮对皮肤完整性确保脑室内接入装置未受损[见剂量和给药方法(2.5)]。
Brineura被禁忌如有急性脑室内接入装置-相关并发症的征象(如,渗漏,装置失效或装置-相关感染的征象例如肿胀,头皮红斑, 液体外渗,或脑室内接入装置周围或上面头皮隆起)[见禁忌证(4)]。脑室内接入装置并发症的情况中,终止Brineura输注和查询装置制造商的说明书为进一步指导。
装置-相关感染的体征和症状可能不明显,所以,CSF样品应常规地被送为测试检测亚临床装置感染[见剂量和给药方法(2.5)]。
临床研究用Brineura中,在两例患者被观察到脑室内接入装置-相关感染。在每个病例,被给予抗菌素,脑室内接入装置被置换,和患继续用Brineura治疗。
脑室内接入装置约105次穿孔后可能发生脑室内接入装置贮存池的的材料降解。脑室内接入装置可能需要立即置换,或前于,Brineura的105次给药,约等同常规给药约4.3年。
5.2 心血管不良反应
开始输注前,输注期间定期地,和输注后在一个卫生保健情况中监视生命征象(血压,心率)[见剂量和给药方法(2.5)]。输注完成时,临床上评估患者状态。如临床上有适应证时可能需要继续观察。
在心动过缓,传导疾患,或有结构性心脏病史患者输注期间进行心电图(ECG)监视,因为有CLN2病有些患者可能发生传导疾患或心脏病。在无心脏异常患者,每6个月应进行常规12-导联ECG评价。
在临床研究中,在2例(8%)患者报告低血压,它发生在Brineura输注期间或至后8小时。患者不需要治疗中变化,和反应自发地或静脉给予液体后解决[见不良反应(6.1)]。
5.3 超敏性反应
临床研究期间Brineura-治疗患者曽报道超敏性反应。输注期间或输注完成的24小时内总共11(46%)患者经受超敏性反应。与超敏性反应同时地观察到体征和症状反应包括发热,呕吐,脑脊液细胞增多或易激惹。Brineura输注前患者被常规地用抗组织胺类有或无解热药或皮质激素预先给药。
由于对过敏反应潜能,当Brineura 被给予时应被容易得到适当的医学支持。如过敏反应发生,立即地终止输注和开始适当医学治疗。输注期间和后严密观察患者。告知患者/护理人员过敏反应的体征和症状,和指导他们发生体征和症状寻求立即医疗护理。
超敏性反应的处根据反应的严重程度和可能包括短暂中断输注,和/或治疗用织胺类,退热药,和/或皮质激素。如发生严重超敏性反应,立即地终止输注和开始适当医学治疗。
6 不良反应
在说明书下面和其他处描述以下不良反应:
● 脑室内接入装置-相关并发症[见警告和注意事项(5.1)]
● 心血管不良反应[见警告和注意事项(5.2)]
● 超敏性反应[见警告和注意事项(5.3)]
6.1 临床试验经验
因为临床试验是在广泛不同情况下进行的,临床试验观察到不良反应率不能与另一种药临床试验发生率直接比较而且可能不反映实践中观察到的发生率。
在24患者有CLN2病接受至少一剂Brineura在一项临床研究有延伸至161周评价Brineura的安全性[见临床研究(14)]。表1总结在Brineura-治疗患者至96周最常见不良反应。
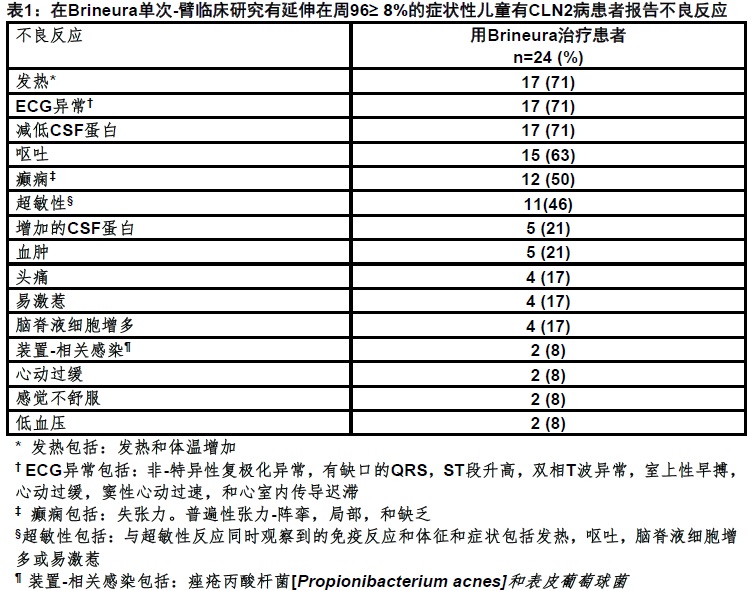
选定的不良反应的描述
癫痫
癫痫被报道在12/24(50%)患者。被报道的癫痫类型包括迟缓型[atonic],全身性强直阵挛[generalized tonic-clonic],局部,和缺乏。癫痫用标准抗惊厥疗法处理和没有导致Brineura治疗的终止。
装置-相关并发症
在12/24(50%)患者观察到与装置相关不良反应。装置-相关不良反应包括 感染,输送系统-相关并发症,和脑脊液细胞增多。这些患者的9例(38%)经历不良反应,它涉及非-植入输送系统组分的并发症。4例患者(16%)有装置-相关不良反应,它需要医学干预,包括两例患者(8%)有脑室内接入装置-相关CNS感染,和1例患者(4%)各有脑室内接入装置的渗漏和脑脊液细胞增多。
通过CSF脑脊液细胞增多增加和微生物学培养和有机体鉴定,无伴随脑膜炎体征和症状诊断装置-相关感染。脑室内接入装置被重置和用抗菌素治疗感染。装置-相关并发症没有导致Brineura治疗的终止[见警告和注意事项(5.1)]。
血肿
在5(21%)用Brineura治疗患者报道血肿不良反应和存在为血肿,程序后血肿,创伤血肿和硬膜下血肿。血肿不需要治疗和不干扰用Brineura输注。
超敏性
尽管用抗组织胺类有或无解热药或皮质激素预先给药在11/24例用Brineura治疗患者(46%)输注期间或Brineura完成后24小时内报道超敏性反应, [见警告和注意事项(5.1)]。观察到大多数常表现同时地与超敏性包括发热与呕吐,脑脊液细胞增多,或易激惹,它不是与经典免疫介导超敏性一致。症状随时间或用给予退热药,抗组织胺类 和/或皮质激素解决和无患者终止用Brineura治疗。
一例患者经受缺氧(用脉冲血氧计减低氧饱和低于88%),Brineura输注8小时后,在输注后15小时接着一个低均数动脉压。给氧后,气道重新定位和生理盐水输注症状解决。一例患者 报告减低氧饱和度(用脉冲血氧计90%),开始Brineura后45分钟伴随底舒张血压。在给氧后缺氧解决。对低舒张血压无治疗被给予,返回至正常而患者继续接受Brineura输注未改变输注速率或剂量。
6.2 免疫原性
如同所有治疗性蛋白,有对免疫原性潜能。抗体形成的检测是高度依赖于分析的灵敏度和特异性。此外,在一个分析中观察抗体阳性的发生率(包括中和抗体)可能受几种因素影响包括 分析方法学,样品处理,采样时机,同时药物,和所患疾病。因为这些理由,比较在下面研
用Brineura治疗患者直至161周在血清和CSF分别都检测到79%和33%对cerliponase alfa的抗-药抗体(ADAs)。经受超敏性不良反应患者被测试对药物-特异性IgE和发现是阴性,包括 三例患者被报道级别3(严重)超敏性 不良反应。血清或CSF ADA滴度和超敏性的发生率或严重程度间未发现关联。未曽评价药物-特异性中和抗体(NAb)。
8 在特殊人群中使用
8.1 妊娠
风险总结
在妊娠妇女中没有关于Brineura可供利用数据告知一个药物-关联妊娠-相关结局的风险。未曽在动物中用cerliponase alfa进行生殖研究。
不知道在适应证人群中重大出生缺陷和流产的估算背景风险。所有妊娠有一个出生缺陷,丢失,或其他不良结局。在美国一般人群,重大出生缺陷和临床上认可妊娠的估算背景风险分别是2至4%和15至20%。
8.2 哺乳
风险总结
在人乳中cerliponase alfa的存在,哺乳喂养婴儿的影响,或对乳汁产生的影响没有数据。哺乳期间缺乏临床数据使之不可能明确确定哺乳期间Brineura对一个婴儿的风险;所以,哺乳喂养对发育和健康的获益应与母亲对Brineura的临床需求和对哺乳喂养婴儿来自Brineura或来自潜在母体情况的任何潜在不良效应一并考虑。
8.4 儿童使用
一项有延伸非-随机化单-臂剂量递增临床研究在有CLN2病患者和来自一个独立自然历史队列有CLN2病未治疗患者比较,研究在3岁和以上有婴儿晚期神经元蜡样脂褐质沉积症2型(CLN2),也被称为三肽氨基肽酶 1(TPP1)缺乏,症状性儿童患者使用Brineura儿童减慢步行的丧失。支持在3岁和以上儿童患者曽确定Brineura的安全性和有效性。[见临床研究(14)]。尚未确定在低于3岁患者安全性和有效性。
11 一般描述
Cerliponase alfa是一种通过重组DNA技术在中国仓鼠卵巢细胞系生产纯化的人酶。活性物质是一种重组人三肽氨基肽酶-1(rhTPP1),一种溶酶体外肽酶。成熟酶的主要活性是宽广范围蛋白质底物N-端三肽的 裂解。Cerliponase alfa含544个氨基酸有一个平均分子质量59 kDa。成熟酶是368个氨基酸长度。在rhTPP1上有5个共识的N-糖基化位点其中含高甘露醇,磷酸化高甘露糖和复合的糖基化结构。
Brineura(cerliponase alfa)注射液和脑室内电解质注射液是通过脑室内输注给药。溶液为无菌,无热原性,和无外来颗粒。Brineura是一种清晰的微乳白色和无色至浅黄色溶液。脑室内电解质是一种清晰至无色溶液。
Brineura和脑室内电解质注射液被包装在10 mL清晰型1一次性-剂量玻璃小瓶[见如何供应/贮存和处置(16)]。每小瓶的Brineura提供5 mL溶液含150 mg cerliponase alfa。每小瓶脑室内电解质注射液提供5 mL溶液。Brineura和脑室内电解质注射液两者都用以下赋形剂被制剂化:二水氯化钙(1.05 mg);六水氯化镁(0.8 mg);氯化钾(1.1 mg);氯化钠(43.85 mg);磷酸氢二钠七水合物(0.55 mg);磷酸钠,单水(0.4 mg);和注射用水,USP。对Brineura溶液的pH of 为6.2至6.8间,和对脑室内电解质注射液为6.0至7.0间。每小瓶含:钠:0.76 mEq,和钾:0.015 mEq。
12 临床药理学
12.1 作用机制
CLN2病是一种神经退行性变性疾病,CNS中溶酶体酶三肽氨基肽酶-1(TPP1)缺乏引起,该酶降解代谢多肽。TPP1无已知的底物特异性。在TPP1活性中缺乏导致在中枢神经系统(CNS)正常地被此酶代谢的物质溶酶体贮存的积蓄,导致运动功能渐进地下降。
Cerliponase alfa(rhTTP1),一种前酶,被CNS中靶细胞摄取和通过阳离子独立的甘露糖-6-磷酸受体[the Cation Independent Mannose-6-Phosphate Receptor](CI-MPR,也被称为M6P/IGF2受体)转位至溶酶体。在溶酶体中Cerliponase alfa被活化和rhTPP1活化的蛋白th水解型的裂解来自蛋白N-端的三肽。
12.3 药代动力学
在有CLN2病患者接受脑室内输注30 mg(0.1倍被批准的推荐剂量),100 mg(约0.3倍批准证的推荐剂量),和300 mg历时约4.5小时每隔一周一次,评价cerliponase alfa的药代动力学。
跨越剂量30 mg,100 mg,和300 mg,初始单次剂量给予后Cerliponase alfa CSF暴露Brineura增加低于正比例性。当Brineura被给予在剂量300 mg每隔一周一次在CSF或血浆无明显cerliponase alfa的积蓄。
Cerliponase alfa 药代动力学有高受试者间和受试者内变异性。在14患者,在天1,周5,和周13,脑室内输注300 mg的Brineura后,表2中总结在CSF和血浆药代动力学参数被评估。
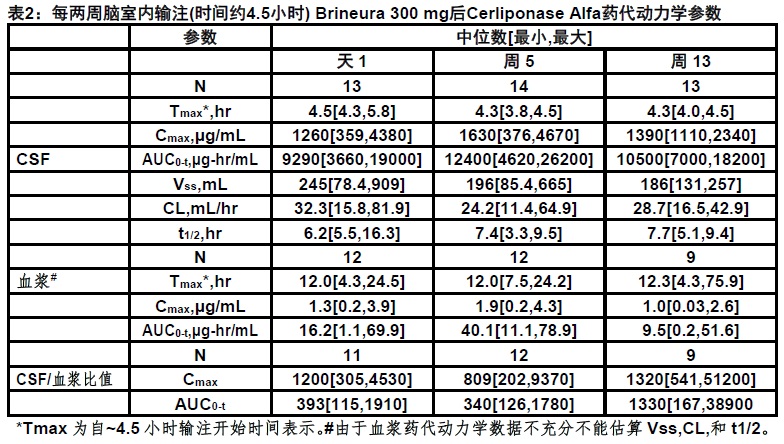
脑室内输注300 mg的Brineura后估算的cerliponase alfa的CSF分布容积(中位Vss = 245 mL)超过典型CSF容积(100 mL)。.
Cerliponase alfa是一种蛋白和预计通过态水解被降解。
13 非临床毒理学
13.1 癌发生,突变发生,生育力受损
未曽用cerliponase alfa进行致癌性,遗传毒性,和生育力研究。根据作用机制,cerliponase alfa期望不是致肿瘤性。
14 临床研究
在一项有延伸期历时96周非随机化单臂剂量递增临床研究在有婴儿晚期神经元蜡样脂褐质沉积症2型(CLN2)病症状性儿童患者中评估Brineura的疗效,被TPP1缺乏确证。
Brineura-治疗患者是与来自自然历史队列未治疗患者比较。CLN2临床计分定量表的运动域[Motor Domain]被用于评估疾病进展。评分范围从3(大略正常)至0(在(走路或爬的能力)丧失运动功能深度地受损位递减,代表里程碑事件。由于有延伸临床研究和自然历史队列间对CLN2语言域计分无法建立可比性,不能确定Brineura对语言域的疗效。
24例患者,年龄3至8岁被纳入Brineura单臂临床研究。63%患者是女性和37%男性。96%患者是高加索人和4%亚裔。一例患者由于不能继续用研究操作一周后撤出;23例患者被用Brineura 300 mg每隔一周一次治疗共48周,和在延伸阶段期间继续治疗。
在有延伸临床研究,在48,72和96时患者被评估在计分定量表的运动域中下降。下降被定义为CLN2临床等级定量表的运动域中有一个非逆转(持续的)2-类别下降或一个非逆转零评分。
如在筛选时一个 组合的运动加语言CLN2低于6评分被记录,患者对Brineura治疗反应被评价。两例患者有一个组合的运动加语言CLN2评分低于6被从分析中排除;在研究阶段自始至终它们保留该评分。在终端时有一个下降患者被早期终止分析。在分析中所用数据来自自然历史队列开始于36个月龄或更大和在首次一个运动加语言CLN2评分低于6被记录时。
在有延伸临床研究中22例Brineura-治疗患者的运动评分与独立的自然历史队列的评分比较,其中包括满足为临床研究纳入标准42例未治疗患者。Logistic模型分析有协变量(筛选年龄,筛选运动评分,基因型:0关键突变(是/否))的结果,显示至96周Brineura-治疗患者没有下降的几率是13倍于自然历史队列患者的没有一个下降几率(成败优势比(95% CI):13.1(1.2,146.9))。
描述性非-随机化比较在一个未校正的非随机化比较,其中22患者用Brineura治疗和评价对 疗效在周96,21例(95%)没有下降,和仅早期终止患者被认为在CLN2临床等级定量表的运动域中有下降趋势。来自自然历史队列结果显示在运动功能中渐进地下降;在自然历史队列中的42患者, 21(50%)经历在历时96周CLN2临床等级定量表的运动域,一个非逆转(持续的) 2-类别下降或非逆转评分为0。
给定非-随机化研究设计,一个Cox 正比例风险模型校正的对年龄,初始运动评分,和基因型 被用于评价在运动域至非逆转2-类别下降或非逆转评分为0时间。这个模型显示在Brineura-治疗患者当与自然历史队列比较在运动功能中较低减低(见图7)。
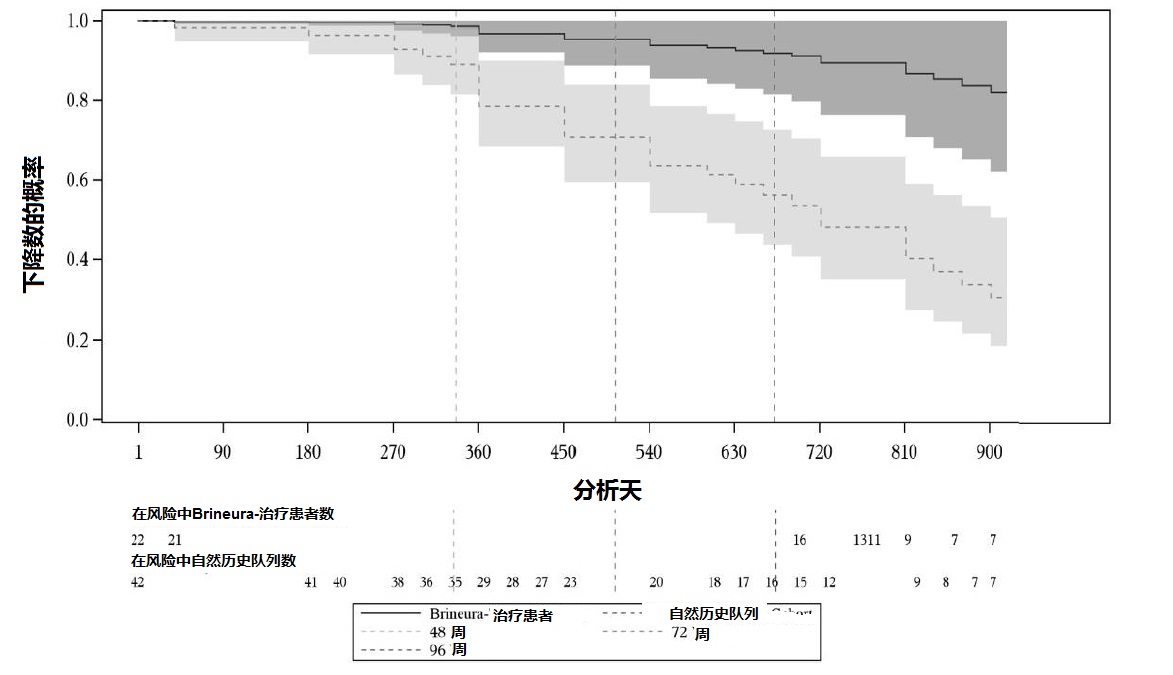
阴影代表95%可信区间
对自然历史队列[natural history cohort]随开始于年龄36个月或更大和在首次一个运动加语言CLN2评分低于6被记录时。
Brineura-治疗人群是完整人群(N=24)减去有基线运动加语言CLN2评分= 6的两患者。
协变量:筛选年龄,筛选运动评分,基因型:0 关键突变(是/否)。“筛选年龄”被定义为在自然历史队列为年龄在一个运动加语言CLN2评分低于6被记录,和不早于36个月龄。自然历史队列的“筛选运动评分”被定义为在筛选年龄时运动评分。
下降被定义为一个非逆转(持续的) 2-类别下降或非逆转零评分在CLN2临床等级定量表中的运动域。
图7. 对非逆转(持续的) 2-类别下降或非逆转评分零在运动域[Motor Domain]估算时间。对症状性儿童患者在Brineura有延伸单臂临床研究和对患者在一个自然历史队列(对协变量根据Cox 正比例风险模型调整)
运动域评分:仅仅匹配的患者进一步评估疗效,22患者来自Brineura临床研究有一个基线组合运动加语言CLN2评分低于6为匹配的对42患者在自然历史队列。患者被匹配根据以下协变量:基线年龄在筛选时3个月内,基因型(0,1,或2 关键突变),和基线运动域 CLN2 评分在筛选时。利用CLN2临床等级定量表的运动域,下降被定义为有一个非逆转2-类别下降或一个零的非逆转评分。在96周时,匹配分析根据17对在运动域对Brineura-治疗患者与在自然历史队列未治疗患者比较显示较少下降(见表3)。
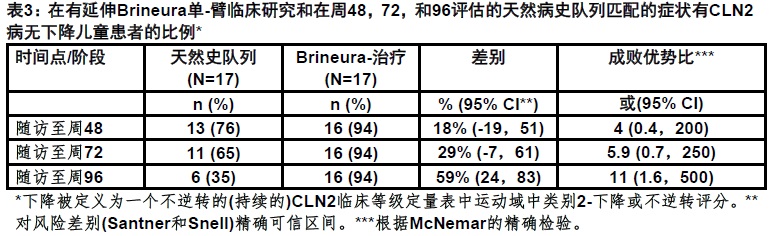
匹配的对基线年龄在筛选3个月内的时间,基因型(0,1,或2关键突变),和在筛选时基线运动域CLN2 评分。
Brineura-治疗人群是根据完整人群减去有基线运动加语言CLN2评分= 6的两例患者。
16 如何供应/贮存和处置
Brineura被供应为一种无菌,清晰至略微乳白色和无色至浅黄色溶液为脑室内输注和脑室内电解质注射液被供应为一种清晰至无色溶液为脑室内输注;两者都被包括在2的包装1。为Brineura使用的给药药盒被分开供应为2的包装2[见剂量和给药方法(2.2)]。
2的包装1
每个Brineura(cerliponase alfa)注射液小瓶有一个绿色的翻转帽(塑料),和含150 mg cerliponase alfa每5 mL(30 mg/mL)。
每个脑室内电解质注射液小瓶 有一个黄色翻转帽(塑料),和含5 mL溶液。
包装1的内容物 NDC号
Brineura(cerliponase alfa)注射液(2小瓶150 mg/5 mL)
脑室内电解质注射液(1小瓶,5 mL) 68135-811-02
2的包装2
为Brineura使用给药药盒被分开供应和含以下一次性-使用, 无菌输注组分:
● 两个20-mL注射器
● 两个注射器针头(21 G,25.4 mm)
● 一条延伸线
● 一个输注组件有0.2 mµ在线过滤器
● 一个端口针(22 G,16 mm)
贮存
Brineura(cerliponase alfa)注射液和脑室内电解质注射液:
贮存直立在冻结箱内(-25°C至 -15°C)在原始纸盒避光保护。
为与Brineura使用给药药盒:
与Brineura分开地贮存在原始纸盒。不要冻结。
17 患者咨询资料
●脑室内接入装置-相关并发症
忠告患者和看护人员装置-相关感染的风险。如存在感染的任何征象,指导患者立即地联系他们的卫生保健提供者[见警告和注意事项(5.1)].
● 心血管不良反应
忠告患者和看护人员Brineura的输注期间和后可能发生低血压和/或心动过缓。指导患者如这些反应发生立即地联系他们的卫生保健提供者[见警告和注意事项(5.2)]。
● 超敏性反应
忠告患者和看护人员可能发生对Brineura治疗相关超敏性反应,包括发热,呕吐,和易激惹。 由于对过敏反应的潜能,告知患者和看护人员过敏反应的体征和症状,和指导他们发生体征和症状应立即寻求医学护理[见警告和注意事项(5.3)]。

