批准日期:20178月3期;公司:AbbVie Inc.
为治疗:慢性丙型肝炎
完整处方资料
1 适应证和用途
MAVYRET是适用为成年患者有慢性丙型肝炎病毒(HCV)基因型1,2,3,4,5或6感染无肝硬化或有代偿的肝硬化(Child-Pugh A)的治疗。MAVYRET还适用为有HCV 基因型1感染成年患者的治疗,患者以前曽被一个含HCV NS5A抑制剂或一个NS3/4A蛋白酶抑制剂(PI)方案治疗,但不是两者[见剂量和给药方法(2.2)和临床研究(14)]。
2 剂量和给药方法
2.1 治疗开始前测试
用MAVYRET开始治疗HCV前测试所有患者对当前或以前的证据HBV感染通过测量乙型肝炎表面抗原(HBsAg)和乙型肝炎核心抗体(抗-HBc)[见警告和注意事项(5.1)]。
2.2 在成年中推荐剂量
MAVYRET是一个固定剂量组合产品在每片含glecaprevir 100 mg和pibrentasvir 40 mg。
MAVYRET的推荐口服剂量是三片(总每天剂量:glecaprevir 300 mg和pibrentasvir 120 mg)每天1次与食物服用[见临床药理学(12.3)]。
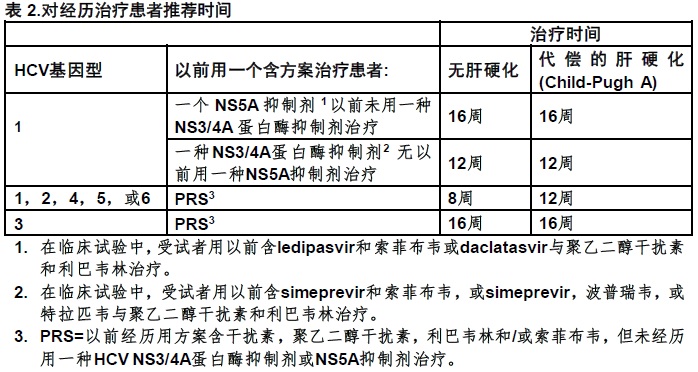
表1和2提供推荐的MAVYRET治疗时间根据患者在HCV单感染的和HCV/HIV-1共感染患者有代偿肝病人群(有或无肝硬化)和有或无肾受损包括患者接受透析。
2.3 肝受损
在有中度肝受损(Child-Pugh B)患者不推荐MAVYRET和在患者有严重肝受损(Child-Pugh C)禁忌[见禁忌证(4),在特殊人群中使用(8.7)和临床药理学(12.3)]。
3 剂型和规格
每片MAVYRET含100 mg的glecaprevir和40 mg的pibrentasvir。片是粉色,椭圆形,膜-包衣,和一侧凹陷有“NXT”。
4 禁忌证
在有严重肝受损(Child-Pugh C)患者禁忌MAVYRET[见剂量和给药方法(2.3),在特殊人群中使用(8.7)和临床药理学(12.3)]。
MAVYRET是禁忌与阿扎那韦或利福平[见药物相互作用(7.3)和临床药理学(12.3)]。
5 警告和注意事项
5.1在患者与HCV和HBV共感染乙型肝炎病毒再活化的风险
乙型肝炎病毒(HBV)再活化曽被报道在HCV/HBV共感染患者正在进行或已完成用HCV直接作用抗病毒药治疗,和患者没有接受HBV抗病毒治疗。有些病例曽导致暴发型肝炎,肝衰竭和死亡。曽报道病例在为HBsAg阳性患者和还有在患者有血清学HBV感染解决的证据(即,HBsAg阴性和抗-HBc阳性)。在接受某些免疫抑制剂或化疗药物患者中也曽报道HBV再活化;在这些患者伴随用HCV直接作用抗病毒药治疗HBV再活化的风险可能被增加。
HBV再活化特征为一个在HBV复制突然增加表现为在血清HBV DNA水平中迅速增加。在患者有已解决的HBV感染中可能发生HBsAg的再出现。肝炎可能伴随HBV复制的再活化,即,转氨酶水平增加和,在严重病例中,胆红素水平增加,可能发生肝衰竭,和死亡。
开始用MAVYRET治疗HCV前通过测量HBsAg和抗- HBc测试所有患者对当前或以前的证据HBV感染。在患者有血清学HBV感染的证据,用MAVYRET治疗HCV期间和治疗后随访期间监视对临床和实验室肝炎复燃或HBV再活化征象。当临床上有适应证时开始对HBV感染适当处理患者。
5.2 由于同时使用MAVYRET与卡马西平,含依法韦仑方案,或圣约翰草减低治疗效应风险
圣约翰草[John’s wort]可能显著地减低glecaprevir和pibrentasvir的血浆浓度,导致减低MAVYRET的治疗效应。不推荐这些药物与MAVYRET使用。
6 不良反应
6.1 临床试验经验
因为临床试验是在广泛不同情况下进行的,临床试验观察到不良反应率不能与另一种药临床试验发生率直接比较而且可能不反映实践中观察到的发生率。
总体不良反应在HCV-感染的成年无肝硬化或有代偿的肝硬化(Child-Pugh A)
在受试者无肝硬化或有代偿的肝硬化(Child-Pugh A) 对MAVYRET不良反应数据是来自九项2和3期试验评价约2,300例受试者感染有基因型1,2,3,4,5,或6 HCV患者接受MAVYRET 共8,12或16周[见临床研究(14)]。
受试者的总体比例永久地终止治疗由于不良反应为0.1%对受试者接受MAVYRET对8,12或16周。
最常见不良反应,所有级别,观察到在大于或等于5%的受试者接受8,12,或16周用MAVYRET治疗为头痛(13%),疲乏(11%),和恶心(8%)。在受试者接受MAVYRET经历不良反应,80% 有一个不良反应轻度严重程度(级别1)。一例受试者经历一个严重的不良反应。
不良反应(类型和严重程度)相似对受试者接受MAVYRET共8,12或16周是相似。不良反应类型和严重程度在受试者有代偿的肝硬化(Child-Pugh A)是与在受试者无肝硬化所见是有可比性。
在用MAVYRET在对照试验被治疗HCV-感染的成年中不良反应
ENDURANCE-2
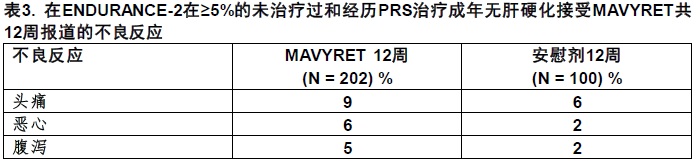
在302例未治疗过或经历PRS治疗中,HCV基因型2感染的成年被纳入在ENDURANCE-2,不良反应(所有强度)发生在至少5%用MAVYRET治疗受试者共12周被展示在表3。在用MAVYRET治疗受试者共12周,32%报道为一个不良反应,其中98%有不良反应轻度至中度严重程度。无用MAVYRET治疗受试者或安慰剂在ENDURANCE-2永久地终止由于一个不良药物反应。
ENDURANCE-3
505例未治疗过,HCV基因型3感染的成年无肝硬化纳入在ENDURANCE-3中,不良反应(所有强度)发生在至少5%的用MAVYRET治疗受试者共8或12周被展示在表4中。在用MAVYRET治疗受试者,45%报道一个不良反应,其中99%有不良反应轻度或中度严重程度。对MAVYRET 8周臂,MAVYRET 12周臂和DCV + SOF臂由于不良反应永久地终止治疗受试者的比例分别为0%,< 1%和1%。
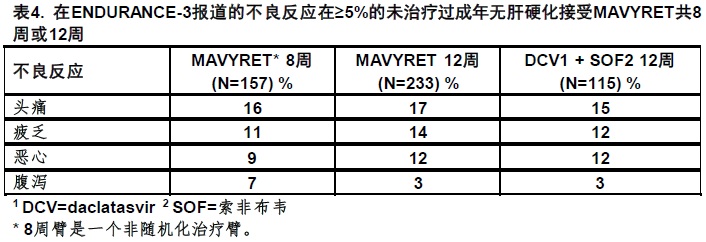
不良反应在HCV-感染的成年有严重肾受损包括受试者用透析
在受试者有慢性肾疾病(期4或期5包括受试者用透析)有基因型1,2,3,4,5或6慢性HCV感染无肝硬化或有代偿的肝硬化(Child-Pugh A)被评估MAVYRET的安全性在104受试者(EXPEDITION-4)接受MAVYRET共12周。观察到最常见不良反应在大于或等于5%受试者接受12周用MAVYRET治疗为瘙痒(17%),疲乏(12%),恶心(9%),无力(7%),和头痛(6%)。在用MAVYRET治疗受试者一种不良反应,90%有不良反应轻度或中度严重程度(级别1或2)。由于不良反应永久地终止治疗受试者的比例为2%。
实验室异常
血清胆红素升高
总胆红素的升高至少2倍正常上限发生在3.5%的用MAVYRET治疗受试者相比0%在安慰剂;观察到跨越2和3期试验这些升高在1.2%受试者。MAVYRET抑制OATP1B1/3和是一种弱UGT1A1抑制剂和可能有潜能影响胆红素转运和代谢,包括直接和间接胆红素。在完成MAVYRET后无受试者经受黄疸和总胆红素水平减低。
7 药物相互作用
7.1 对MAVYRET对其他药物潜在影响的机制
Glecaprevir和pibrentasvir是P-糖蛋白(P-gp),乳癌耐药蛋白(BCRP),和有机阴离子转运多肽(OATP)1B1/3的抑制剂。与MAVYRET共同给药可能增加P-gp,BCRP,OATP1B1或OATP1B3底物药物的血浆浓度。Glecaprevir和pibrentasvir是细胞色素P450(CYP) 3A,CYP1A2,和尿苷萄糖醛酸基转移酶(UGT) 1A1的弱抑制剂
7.2 对其他药物对MAVYRET潜在影响的机制
Glecaprevir和pibrentasvir是P-gp和/或BCRP的底物。Glecaprevir是一种OATP1B1/3的底物。MAVYRET与药物抑制肝P-gp,BCRP,或OATP1B1/3的共同给药可能增加glecaprevir和/或pibrentasvir的血浆浓度.
MAVYRET与药物诱导P-gp/CYP3A的共同给药可能减低glecaprevir和pibrentasvir血浆浓度。
卡马西平,依法韦仑,和圣约翰草可能显著地减低glecaprevir和pibrentasvir的血浆浓度,导致减低MAVYRET的治疗效应。不推荐这些药物与MAVYRET使用[见警告和注意事项(5.2)和临床药理学(12.3)]。
7.3 确定的和其他潜在的药物相互作用
表5提供MAVYRET对共同给药药物浓度的影响和共同给药药物对glecaprevir和pibrentasvir的影响[见禁忌证(4)和临床药理学(12.3)].
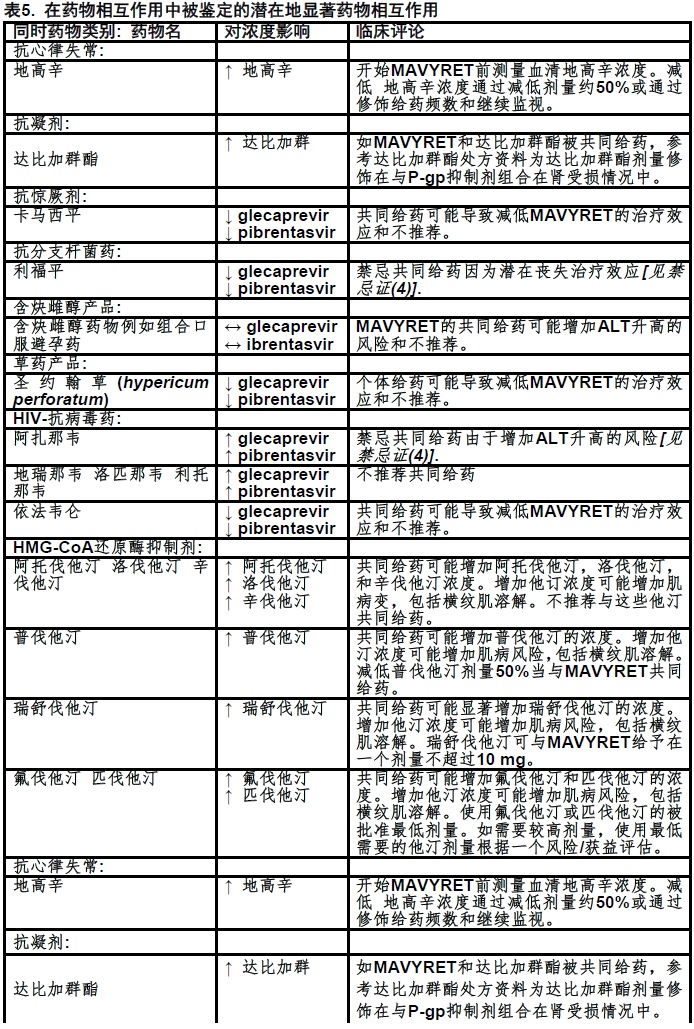
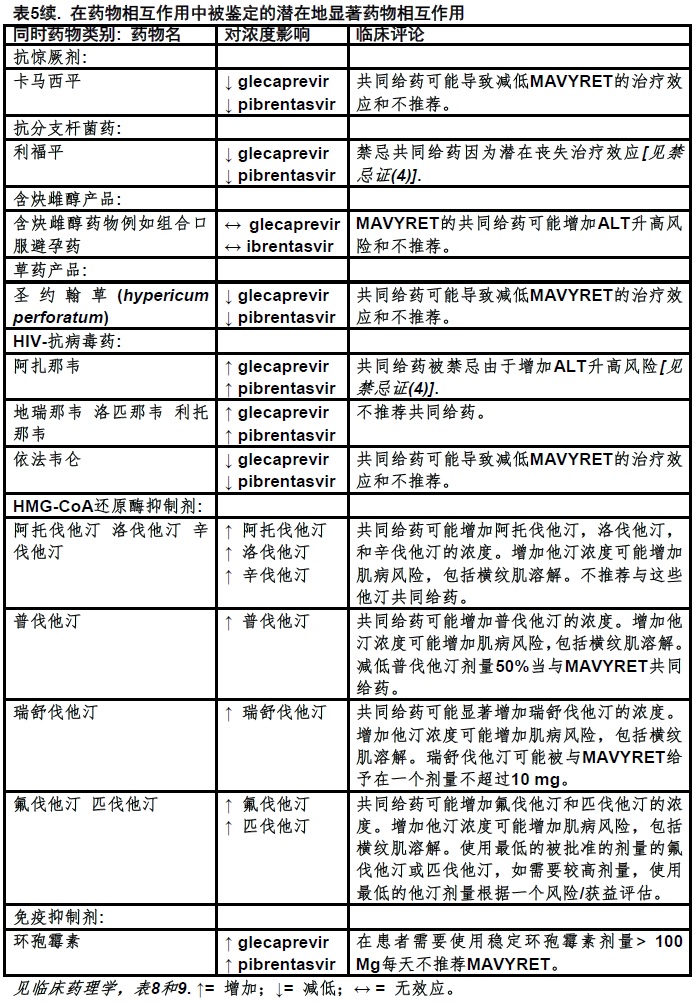
7.4 没有观察到与MAVYRET临床上显著相互作用的药物
当MAVYRET与以下药物共同给药无需剂量调整:阿巴卡韦,氨氯地平[amlodipine],丁丙诺啡[buprenorphine],咖啡因,右美沙芬,dolutegravir,埃替拉韦/cobicistat,恩曲他滨,非洛地平[felodipine],拉米夫定,拉莫三嗪[lamotrigine],氯沙坦,美沙酮[methadone],米达唑仑[midazolam],纳洛酮[naloxone],炔诺酮[norethindrone]或其他仅孕激素避孕药,奥美拉唑,雷特格韦[raltegravir],利匹韦林[rilpivirine],索非布韦,他克莫司[tacrolimus],替诺福韦甲酰胺[tenofovir alafenamide],富马酸替诺福韦酯[tenofovir disoproxil fumarate],甲苯磺丁脲[tolbutamide],和缬沙坦[valsartan].
8 在特殊人群中使用
8.1 妊娠
风险总结
没有适当人数据可得到以确定MAVYRET是否对妊娠结局具有一个风险。在动物生殖研究,当MAVYRET组分在器官形成期间分开地给予在暴露至53倍未观察到不良发育效应(大鼠; glecaprevir)或51和1.5倍(分别小鼠和兔;pibrentasvir)人暴露在MAVYRET的推荐剂量[见数据]。在兔中有关glecaprevi潜在的发育效应不能做确定结论,因为在这个品种中最高的实现glecaprevir暴露仅为7%(0.07倍)的人暴露在推荐剂量。There were no effects 用任何 eit一个化合物在啮齿类围产期发育研究其中母体对glecaprevir和pibrentasvir全身暴露(AUC)分别为在人在推荐剂量时暴露约47和74倍[见数据]。
不知道对适应证人群重大出生缺陷和流产背景的风险。在美国一般人群,重大出生缺陷和在临床上认可妊娠中流产的估算背景的风险分别是2%至4%和15%至20%。
Glecaprevir
Glecaprevir被口服地给予至妊娠大鼠(直至120 mg/kg/day)和兔(直至60 mg/kg/day)在器官形成阶段期间(妊娠天(GD)分别6至18,和GD 7至19)。在直至未观察到不良胚胎-胎儿效应在大鼠在给药水平直至120 mg/kg/day(53倍暴露在人在推荐人剂量(RHD))。在兔中,最高的glecaprevir暴露实现为7%(0.07倍)的暴露在人在RHD。就其本身而言,数据在兔中在器官形成期间是不能得到对glecaprevir全身暴露在或高于暴露在人在RHD时。.
在大鼠中,在围产期发育研究,glecaprevir被口服地给予(直至120 mg/kg/day)从GD 6至哺乳天20。在母体暴露47倍在人在RHD暴露未观察到效应。
Pibrentasvir
Pibrentasvir在器官形成阶段期间被口服给予妊娠小鼠和兔(直至100 mg/kg/day)(分别GD 6至15,和GD 7至19)。在任何品种在任何研究剂量水平无不良胚胎-胎儿效应。最高剂量全身暴露为51倍(小鼠)和1.5倍(兔)在人中在RHD中暴露。在小鼠围产期发育研究中,pibrentasvir被口服地给予(直至100 mg/kg/day)从GD 6至哺乳天20。在母体暴露约74倍人中在RHD暴露未观察到效应。
8.2 哺乳
风险总结
不知道MAVYRET的组分是否被排泄在人哺乳乳汁,影响人乳汁生产,或有效应对哺乳喂养婴儿。当给予至哺乳啮齿类, MAVYRET的组分存在乳汁中,在哺乳幼崽中未观察到对生长和发育影响[见数据]。
哺乳喂养发育和健康获益应被与母亲对MAVYRET的临床需求和哺乳喂养儿童来自MAVYRET或来自母体潜在条件任何潜在不良效应一并考虑。
数据
在最高测试剂量(对glecaprevir120 mg/kg/day和对pibrentasvir 100 mg/kg/day)在哺乳幼崽未观察到glecaprevir或pibrentasvir对生长和产后发育显著影响。母体全身暴露(AUC)于glecaprevir和pibrentasvir分别为约47或74倍在人RHD时暴露。在产后天14在哺乳幼崽中对glecaprevir全身暴露为约0.6至2.2 %母体暴露和对pibrentasvir约母体暴露的四分之一至三分之一。
Glecaprevir或pibrentasvir被给予至(单剂量;5 mg/kg口服)至哺乳大鼠,8至12天产后。Glecaprevir在乳汁中为13倍较低于血浆和pibrentasvir在乳汁为1.5倍较高于血浆。在乳汁中母体药物(glecaprevir或pibrentasvir)代表多数(>96%)总体药物-相关物质。
8.4 儿童使用
尚未确定在低于18岁儿童中MAVYRET的安全性和有效性。
8.5 老年人使用
在MAVYRET的临床试验中,328例受试者为年龄65岁和以上(在2和3期临床试验受试者的总这些受试者和较年轻受试者间未观察到安全性或有效性中总体差别,而其他报告的临床经验没有鉴定老年和较年轻受试者间反应中差别。在老年患者没有证明MAVYRET剂量调整是正当[见临床药理学(12.3)]。
8.6 肾受损
在有轻度,中度或严重肾受损,包括那些用透析患者无需MAVYRET的剂量调整[见临床药理学(12.3)和临床研究(14.5)]。
8.7 肝受损
在有轻度肝受损(Child-Pugh A)患者中MAVYRET是无需剂量调整。不推荐在有中度肝受损(Child-Pugh B)患者用MAVYRET。尚未确定在HCV-感染的有中度肝受损患者中的安全性和疗效。在有严重肝受损(Child-Pugh C)患者由于glecaprevir和pibrentasvir的较高暴露MAVYRET是被禁忌[见剂量和给药方法(2.3),禁忌证(4),和临床药理学(12.3)]。
10 药物过量
在过量的情况中,患者应被监视对毒性的任何体征和症状。应立即开始适当对症治疗。Glecaprevir和pibrentasvir不被血液透析显著地去除。
11 一般描述
MAVYRET是一个固定剂量组合片含glecaprevir和pibrentasvir为口服给药。Glecaprevir是一种HCV NS3/4A 蛋白酶抑制剂,而pibrentasvir是一个HCV NS5A抑制剂。
Glecaprevir/Pibrentasvir膜-包衣的立即释放片
每片含100 mg的glecaprevir和40 mg的pibrentasvir。Glecaprevir和pibrentasvir是作为一个共制剂,固定剂量组合,立即释放双层片存在。
片含以下无活性成分:胶体二氧化硅,共聚维酮(type K 28),交联羧甲基纤维素钠,羟丙甲纤维素2910,氧化铁红,乳糖一水化物,聚乙二醇3350,丙二醇单辛酸酯(类型II),硬脂酰富马酸钠,二氧化钛,和维生素E(生育酚)聚乙二醇琥珀酸。
片不含麸质。
Glecaprevir药物物质:
Glecaprevir的化学名为(3aR,7S,10S,12R,21E,24aR)-7-tert-butyl-N-{(1R,2R)-2(difluoromethyl)-1-[(1-methylcyclopropane-1-sulfonyl)carbamoyl]cyclopropyl}-20,20-difluoro5,8-dioxo-2,3,3a,5,6,7,8,11,12,20,23,24a-dodecahydro-1H,10H-9,12methanocyclopenta[18,19][1,10,17,3,6]trioxadiazacyclononadecino[11,12-b]quinoxaline-10carboxamide hydrate.
分子式为C38H46F4N6O9S(无水化合物)和对药物物质的分子量为838.87 g/mol(无水化合物). Glecaprevir的强度是根据无水glecaprevir。Glecaprevir是一种白色至灰白色结晶性粉末有一个溶解度低于0.3 mg/mL跨越一个pH范围2–7在37°C和是实际上不溶于水,但微溶于乙醇。 Glecaprevir有以下分子结构。
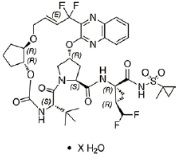
Pibrentasvir药物物质:
Pibrentasvir的化学名为Methyl {(2S,3R)-1-[(2S)-2-{5-[(2R,5R)-1-{3,5-difluoro-4[4-(4-fluorophenyl)piperidin-1-yl]phenyl}-5-(6-fluoro-2-{(2S)-1-[N-(methoxycarbonyl)-Omethyl-L-threonyl]pyrrolidin-2-yl}-1H-benzimidazol-5-yl)pyrrolidin-2-yl]-6-fluoro-1Hbenzimidazol-2-yl}pyrrolidin-1-yl]-3-methoxy-1-oxobutan-2-yl}carbamate.
对药物物质的分子式为C57H65F5N10O8和分子量为1113.18 g/mol。Pibrentasvir是淡黄色一种白色至灰白色至淡黄色结晶粉有一个溶解度低于0.1 mg/mL跨越Ph范围1–7在37°C和是实际上不溶于水,但自由地溶于乙醇。Pibrentasvir有以下分子结构: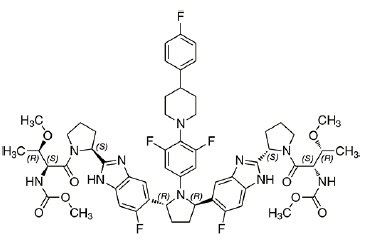
12 临床药理学
12.1 作用机制
MAVYRET是一种glecaprevir和pibrentasvir的固定剂量组合,它是对丙型肝炎病毒直接作用抗病毒药物[见微生物学(12.4)]。
12.2 药效动力学
心脏电生理学
剂量直至glecaprevir 600 mg的效应(2倍推荐剂量)与剂量直至pibrentasvir 240 mg(2倍推荐剂量)对QTc间期被评价在一项阳性对照(莫西沙星[moxifloxacin] 400 mg)彻底QT研究。在20-倍的glecaprevir和5倍的pibrentasvir治疗浓度,glecaprevir和pibrentasvir组合不延长QTc间期至任何临床上相关程度。
12.3 药代动力学
在表6中提供在健康受试者中MAVYRET组分的药代动力学性质。在表7中提供glecaprevir和pibrentasvir在HCV-感染的无肝硬化受试者中稳态药代动力学参数。
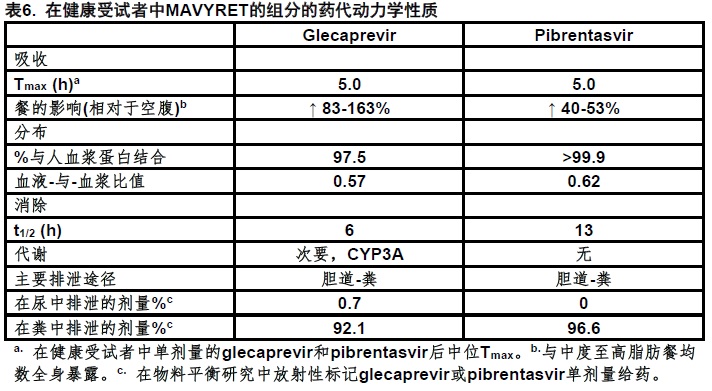
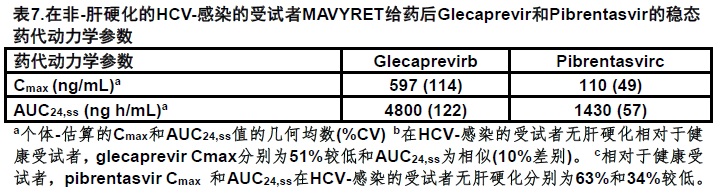
特殊人群
儿童患者
尚未确定在儿童患者中MAVYRET的药代动力学。
受试者有肾受损
在非-HCV感染的受试者有轻度,中度,严重,或肾受损终末期(估算的GFR利用修饰的膳食在肾病)没有用透析与有正常肾功能受试者比较Glecaprevir和pibrentasvir AUC被增加≤ 56%。在透析-依赖非-HCV感染的受试者有和无透析Glecaprevir和pibrentasvir AUC为相似(≤ 18%差别)。在HCV-感染的受试者,对受试者有肾病终末期,有或无透析,与受试者有正常肾功能比较观察到86%较高的glecaprevir和54%较高的pibrentasvir AUC。
有肝受损受试者
在HCV感染的受试者有代偿的肝硬化(Child-Pugh A)MAVYRET的给药后,glecaprevir的暴露为约2-倍和pibrentasvir暴露为相似于非-肝硬化HCV感染的受试者。
在临床剂量,与有正常肝功能非-HCV感染的受试者比较,glecaprevir AUC 100%较高在Child-Pugh B受试者,和增加至11-倍在Child-Pugh C受试者。Pibrentasvir 为26%较高在Child-Pugh B受试者,和114%较高在Child-Pugh C受试者。
年龄/性别/种族/体重
根据年龄[18-88岁],性别,种族/民族或体重未观察到glecaprevir或pibrentasvir的药代动力学中临床意义差别。
药物相互作用研究
用glecaprevir/pibrentasvir和其他很可能被共同给药药物和用药物常被用作为探针为药代动力学相互作用进行药物相互作用研究。表8和9总结了药代动力学影响当glecaprevir/pibrentasvir被共同给予与其他药物它显示潜在临床相关变化。当MAVYRET是与CYP3A,CYP1A2,CYP2C9,CYP2C19,CYP2D6,UGT1A1,或UGT1A4的底物共同给药不期望显著相互作用。
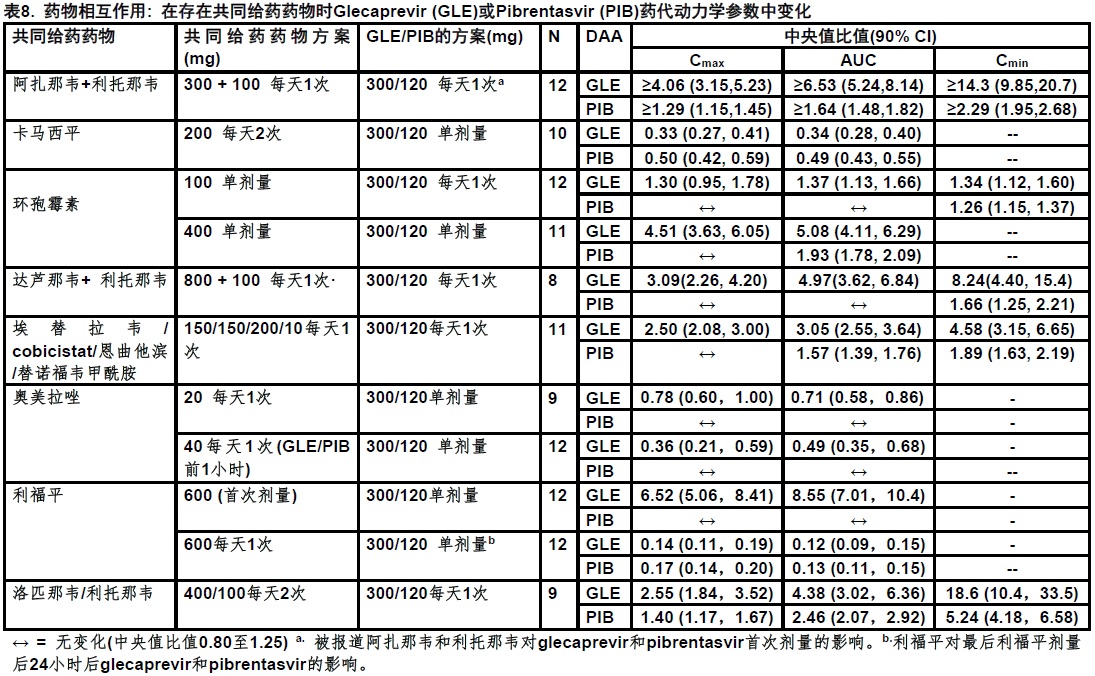
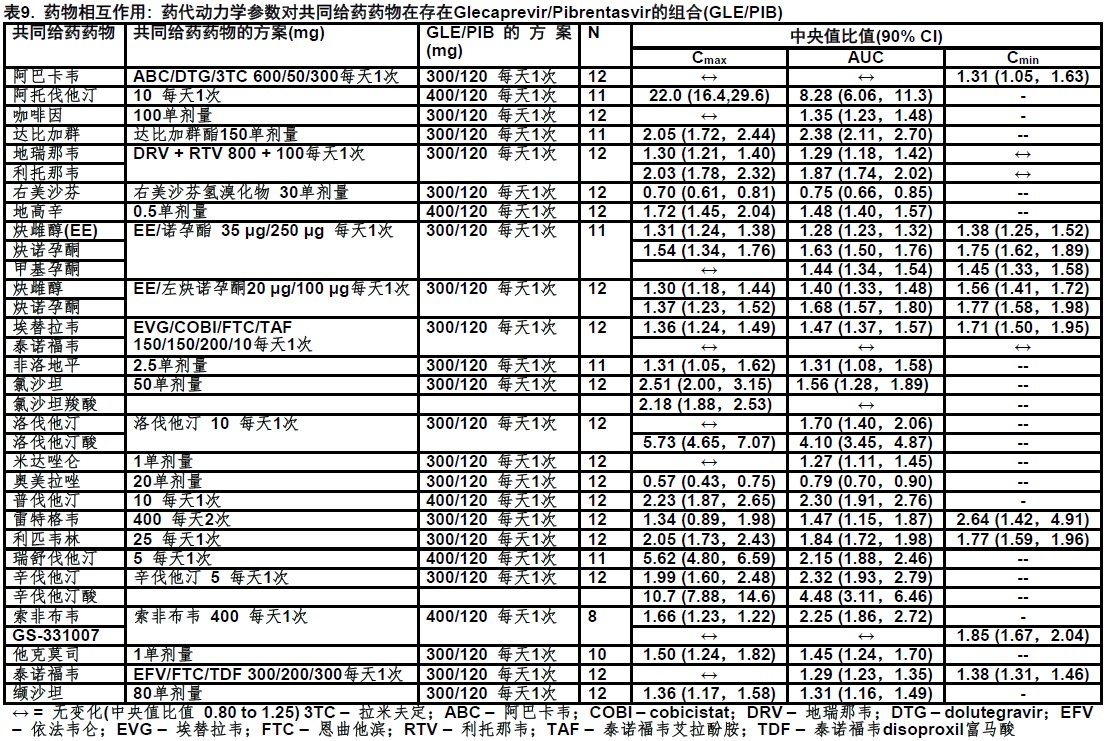
12.4 微生物学
作用机制
Glecaprevir
Glecaprevir是一种HCV NS3/4A蛋白酶的抑制剂,它是为HCV编码多蛋白的蛋白水解裂解需要(至NS3,NS4A,NS4B,NS5A,和NS5B蛋白的成熟型)和是对病毒复制必不可少。在一项生化分析中,glecaprevir抑制来自HCV基因型1a,1b,2a,2b,3a,4a,5a,和6a重组NS3/4A酶分离株的蛋白水解活性有IC50 值范围从3.5至11.3 nM。
Pibrentasvir
Pibrentasvir是HCV NS5A的一种抑制剂,它是对病毒RNA复制和病毒颗粒组装必不可少。Pibrentasvir的作用机制曽根据细胞培养抗病毒活性和耐药性图研究曽被特征化。
抗病毒活性
在HCV复制子分析中,glecaprevir有中位EC50值of 0.08-4.6 nM对实验室和临床分离株来自亚型1a,1b,2a,2b,3a,4a,4d,5a,和6a。Pibrentasvir有中位EC50值0.5-4.3 pM对实组合抗病毒活性
Glecaprevir和pibrentasvir的组合的评价显示在细胞培养分析中在抗病毒活性中无拮抗作用。
耐药性
在细胞培养中
HCV 基因型1a,1b,2a,3a,4a或6a复制子的选择对glecaprevir减低易感性导致氨基酸取代的出现最常见在NS3位置A156或D/Q168。在NS3氨基酸位置A156 引入至HCV复制子个体取代通过指向位点-突变一般地生成致最大地减低(>100倍)在对glecaprevir易感性。在NS3位置个体取代D/Q168对glecaprevir易感性有不同效应依赖于HCV基因型/亚型和特异性氨基酸变化,有最大减低(>30-倍)观察到在基因型1a(D168F/Y),3a(Q168R)和6a(D168A/G/H/V/Y)。NS3 Y56H加D/Q168的组合取代较大减低在glecaprevir易感性。一个NS3 Q80R取代在基因型3a致一个21-倍减低在glecaprevir易感性,而Q80取代在基因型1a和1b(包括基因型1a Q80K)不减低glecaprevir易感性。个体氨基酸取代个体氨基酸耐药性对其他HCV蛋白酶抑制剂在位置36,43,54,55,56,155,166,或170在NS3中一般地不减低对glecaprevir易感性。
HCV基因型1a,2a或3a复制子的选择对减低对pibrentasvir易感性导致氨基酸取代的出现在已知的NS5A抑制剂耐药性-伴随位置,包括Q30D/缺失,Y93D/H/N或H58D +Y93H在基因型1a复制子,F28S + M31I或P29S + K30G在基因型2a复制子,额Y93H在基因型3a复制子。个体氨基酸取代的多数个体氨基酸耐药性对其他HCV NS5A抑制剂在位置24,28,30,31,58,92,或93在NS5A不减低对pibrentasvir易感性。个体NS5A氨基酸取代减低对pibrentasvir易感性包括M28G或Q30D在一个基因型1a复制子(分别244-和94倍),和P32-缺失在一个基因型1b复制子(1,036-倍)。两个或更多NS5A抑制剂耐药性-伴随氨基酸取代的有些组合可能导致在pibrentasvir易感性更大减低。
在临床研究中
在未治疗过和聚乙二醇干扰素,利巴韦林和/或索非布韦治疗-经受受试者有或无肝硬化研究
两个基因型1-被感染的受试者经历病毒学失败中,两例受试者有一个亚型1a感染。一例受试者有治疗-出现取代A156V在NS3,和Q30R,L31M和H58D在NS5A(在基线时也被检测到一个低频数Q30R和L31M)一例受试者有治疗-出现Q30R和H58D(而在基线和治疗后存在Y93N) 在NS5A。
两个基因型2-感染的受试者中经历病毒学失败,两例受试者有一个亚型2a感染,而在NS3或NS5A未观察到治疗-出现取代。
18例基因型3-感染的受试者中经历病毒学失败,在11受试者观察到治疗-出现NS3取代Y56H/N,Q80K/R,A156G,或Q168L/R。在5受试者在和治疗后存在基线一个166S或Q168R。在16受试者观察到治疗-出现NS5A取代M28G,A30G/K,L31F,P58T,或Y93H,和13例受试者在基线和治疗后有A30K(n=9)或Y93H(n=5)。
在受试者有或无肝硬化患者为治疗-经历对NS3/4A蛋白酶和/或NS5A抑制剂研究
对11例HCV基因型1感染的受试者(10基因型1a,1基因型1b)有以前NS3/4A蛋白酶抑制剂[PI]或NS5A抑制剂治疗经验患者经历用MAVYRET有或无利巴韦林病毒学失败在MAGELLAN-1研究进行治疗-出现耐药性分析。在73%(8/11)受试者观察到治疗-出现NS3取代V36A/M,Y56H,R155K/T,A156G/T/V,或D168A/T。9/10受试者(90%,不包括一例在失败时受试者缺失NS5A数据)有治疗-出现NS5A取代M28A/G(或L28M对基因型1b),P29Q/R,Q30K/R,H58D或Y93H/N。所有11例受试者还有NS5A抑制剂耐药性关联取代缺失在基线时,和7/11 有NS3蛋白酶[PI]耐药性关联取代缺失在基线时(见交叉-耐药性 for the effect of 基线耐药性关联取代对治疗反应对NS3/4A PI或NS5A抑制剂治疗-经历患者).
基线HCV氨基酸多态性对治疗反应的影响(NS3/4A PI-和NS5A抑制剂-未治疗过受试者)
NS3/4A蛋白酶[PI]-和NS5A抑制剂-未治疗过受试者接受MAVYRET在2期和3期临床研究进行确定HCV亚型代表和开拓基线氨基酸多态性和治疗结局间关联的合并分析。基线多态性 相对于一个亚型特异性参比序列在耐药性-关联氨基酸位置155,156,和168在NS3,和24,28,30,31,58,92,和93在NS5A被评价在一个15%检测的受试者有HCV基因型1,2,3,4,5,和6感染。跨越所有基因型未检测到在NS3氨基酸位置156基线多态性。分别在27%(225/841),80%(331/415),22%(136/615),50%(80/161),13%(4/31),和54%(20/37)的HCV基因型1,2,3,4,5,和6感染受试者检测到在NS5A基线多态性。
基因型1,2,4,5,和6:基线HCV多态性在基因型1,2,4,5和6对治疗结局没有影响。
基因型3:在未治疗过,基因型3-感染的受试者无肝硬化接受MAVYRET共8周,一个NS5A A30K多态性被检测到在10%(18/181)的受试者中,其中78%(14/18)实现SVR12。得到的不充分数据不能描述A30K多态性在基因型3-感染的受试者有肝硬变(n=1,SVR12)或以前经历治疗(n=1,复发)患者接受推荐的MAVYRET方案的影响。所有基因型3-感染的受试者(100%,16/16)有Y93H在NS5A在基线时患者接受推荐的MAVYRET方案实现SVR12。
交叉-耐药性
观察到根据耐药性模在细胞培养复制子研究和HCV-被感染的受试者,glecaprevir和其他 HCV NS3/4A蛋白酶抑制剂[PIs]间,和pibrentasvir和其他HCV NS5A 抑制剂间交叉-耐药性是可能性。 MAVYRET和索非布韦,聚乙二醇干扰素或利巴韦林间不期望交叉-耐药性。
在MAGELLAN-1研究,HCV基因型1-感染的受试者曽以前用NS3/4A蛋白酶和/或NS5A抑制剂被治疗用MAVYRET共12或16周治疗曽失败。用下一代测序 在15%检测阈基线序列被分析。
在23例NS3/4A蛋白酶抑制剂[PI]-经历/NS5A 抑制剂-未治疗过受试者中接受MAVYRET共12周在MAGELLAN-1(排除2例非-病毒学失败受试者),2例受试者各自有基线NS3 R155K或D168E/V取代;所有23例受试者实现SVR12。
经历NS5A抑制剂/蛋白酶抑制剂[PI]-未治疗过受试者中接受MAVYRET共16周,基线NS5A 耐药性关联取代[R30Q(n=1),Y93H/N(n=5),M28A+Q30R(n=1),Q30H+Y93H(n=1),Q30R+L31M(n=2),L31M+H58P(n=1)],被检测在73%(11/15)受试者有可得到的数据,其中91%(10/11)实现SVR12。非-SVR12受试者经历用-治疗病毒学失败和有一个基因型1a感染与基线NS5A Q30R和L31M取代。
耐药性关联取代的持久性
不能得到关于glecaprevir和pibrentasvir耐药性关联取代的持久性的数据。用其他NS5A抑制剂治疗的患者观察的NS5A 耐药性关联曽被发现持续共长于一年。在用其他NS3/4A 蛋白酶抑制剂[PI]治疗患者,有NS3 耐药性关联取代病毒群曽被发现下降在有些患者至治疗后周24和48。不知道含glecaprevir或pibrentasvir 耐药性关联取代病毒出现或持久性的长期临床影响。
13 非临床毒理学
13.1 癌发生,突变发生,生育力受损
癌发生和突变发生
Glecaprevir和pibrentasvir没有遗传毒性在一组体外或体内分析,包括细菌致突变性,利用人外周血淋巴细胞染色体畸变和体内啮齿类微核试验。.
未曽用glecaprevir和pibrentasvir进行致癌性研究。
生育力受损
在啮齿类直至最高测试剂量未观察到对交配,雌性或雄性生育力,或早期胚胎发育无影响。对glecaprevir和pibrentasvir全身暴露(AUC)较高于在人中在推荐剂量的暴露分别为约 63和102倍。
14 临床研究
14.1 临床试验的描述
表10总结了临床试验进行支持在受试者有HCV基因型1,2,3,4,5或6感染和代偿肝疾病(包括Child-Pugh A肝硬变)按照治疗史和肝硬变状态的MAVYRET有效性。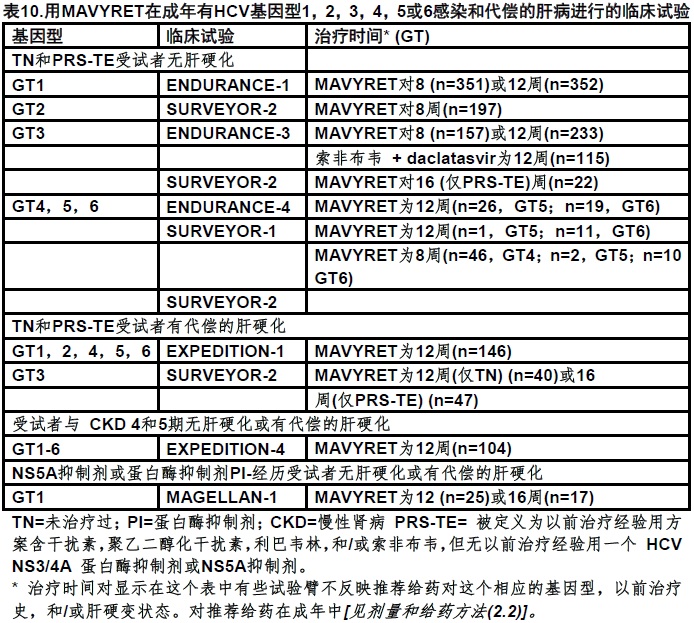
血清HCV RNA值被测量临床试验期间利用Roche COBAS AmpliPrep/COBAS Taqman HCV 测试(版本2.0)用一个定量(LLOQ)低限15 IU/L(除了对SURVEYOR-1和SURVEYOR-2 它们用Roche COBAS TaqMan实时逆转录酶-PCR(RT-PCR)分 v. 2.0用一个LLOQ为25 IU/mL)。主要终点一个交叉所有临床试验为持续病毒学反应(SVR12),被定义为HCV RNA被低于LLOQ在治疗结束后12周。复发被定义为HCV RNA ≥ LLOQ治疗反应的结束后完成治疗受试者中。受试者有缺失HCV RNA数据,例如那些患者终止由于一个不良事件,受试者撤出或为丧失随访,被计为SVR12失败。.
临床试验的人口统计和基线特征在未治疗过或经历治疗成年对聚乙二醇干扰素,利巴韦林和/或索非布韦(PRS)无肝硬化或有代偿的肝硬化(Child-Pugh A)
2,152例被治疗的受试者无肝硬化或有代偿的肝硬化患者为未治疗过或经历-干扰素,聚乙二醇干扰素,利巴韦林和/或索非布韦(PRS)组合治疗中,排除EXPEDITION-4和MAGELLAN-1,中位年龄为54岁(范围:19至88);73%为未治疗过,27%为经历PRS;39%为HCV基因型1;21%为HCV基因型2;29%为HCV基因型3;7%为HCV基因型4;4%为HCV基因型5-6;13%为≥65岁;54%为男性;5%为黑种人;12%有肝硬变;20%有机体质量指数至少30 kg每m2;和中位基线HCV RNA水平为6.2 log10 IU/mL。
14.2未治疗过或PRS治疗-经历成年有HCV基因型1,2,4,5,或6感染无肝硬化
MAVYRET的疗效在受试者为未治疗过或经历治疗对聚乙二醇干扰素,利巴韦林和/或索非布韦(PRS)的组合有基因型1,2,4,5或6 慢性HCV感染无肝硬化被研究在四项试验利用8-或12-周时间:ENDURANCE-1,ENDURANCE-4,SURVEYOR-1(部分2),和SURVEYOR-2(部分2和部分 4).
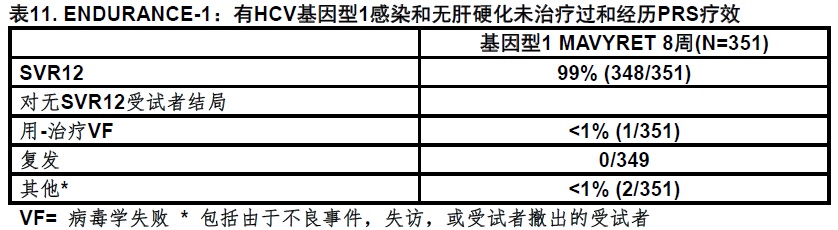
ENDURANCE-1为一项随机化(1:1),开放,多-国家试验比较 用MAVYRET8周治疗疗效相比在无肝硬化有基因型1感染有或无HIV-1共感染受试者治疗12周(n=33共感染)。表11展示在MAVYRET-被治疗基因型1感染的受试者共8周治疗臂中SVR12。由于数字上相似的疗效,MAVYRET被推荐共8周为未治疗过和PRS治疗-经历基因型1受试者无肝硬化,而不是12周[见剂量和给药方法(2.2)]。
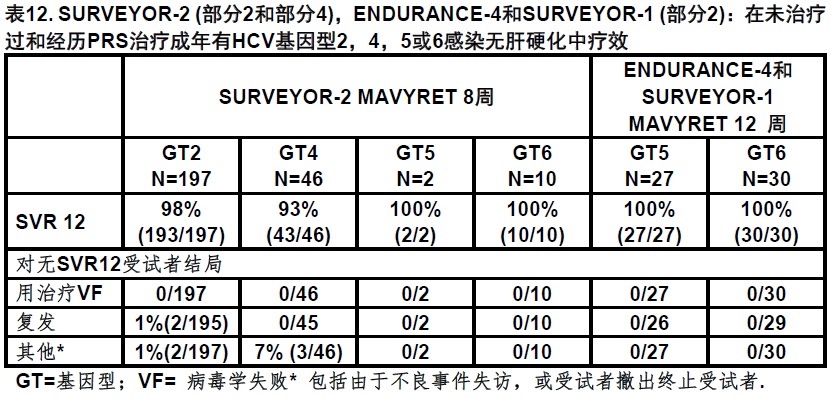
5,或6感染的有代偿的肝硬化
在单-臂,开放EXPEDITION-1试验,其中包括146例用MAVYRET治疗受试者共12周研究有基因型1,2,4,5或6慢性丙型肝炎病毒感染的有代偿的肝硬化(Child-Pugh A)研究在受试者是未治疗过或经历治疗对聚乙二醇干扰素,利巴韦林和/或索非布韦(PRS)的组合中MAVYRET的疗效。
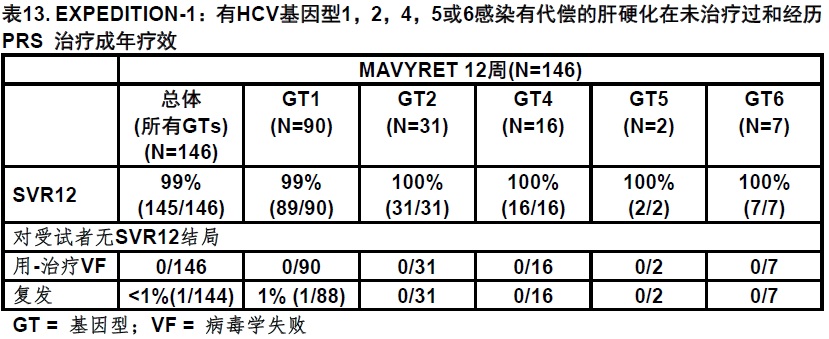
14.4 未治疗过或经历PRS治疗-成年有HCV基因型3感染无肝硬化或有代偿的肝硬化
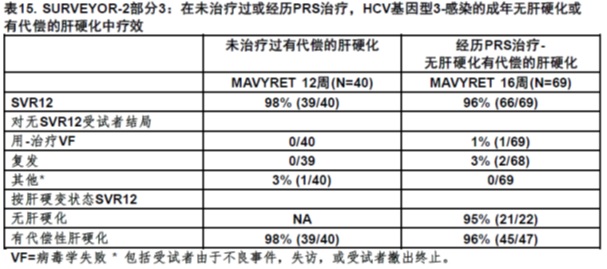
在ENDURANCE-3和在SURVEYOR-2部分3中在受试者无肝硬化或有代偿的肝硬化患者为未治疗过或经历聚乙二醇干扰素,利巴韦林和/或索非布韦(PRS)组合治疗的有基因型3慢性HCV感染研究MAVYRET的疗效。
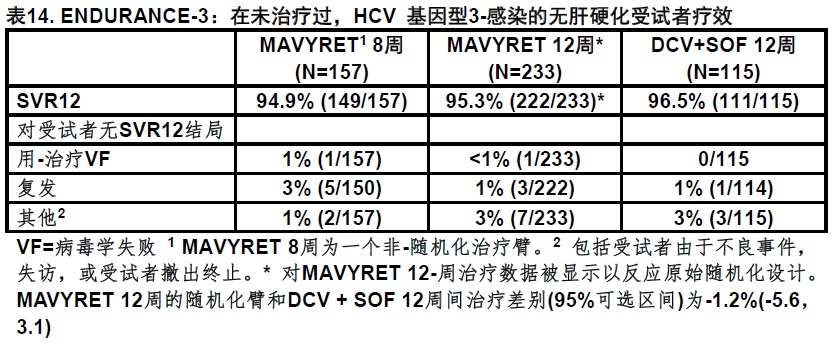
ENDURANCE-3为一项在未治疗过受试者部分地-随机化,开放,阳性-对照试验。受试者被随机化(2:1)至或MAVYRET共12周或至索非布韦和daclatasvir的组合共12周;随后地试验包括一个第三个非-随机化臂用MAVYRET共8周。在表14总结SVR12数据。由于数字上相似疗效MAVYRET被推荐共 8周为治疗未治疗过基因型3 受试者无肝硬化,而不是12周[见剂量和给药方法(2.2)]。
MAVYRET 12周和DCV + SOF 12周的随机化臂.
SURVEYOR-2部分3是一项开放试验随机化经历PRS治疗-受试者有基因型3感染无肝硬化至12-或16-周的治疗。此外,试验在基因型3感染的受试者有代偿的肝硬化在两个专门治疗臂利用12-周(仅-未治疗过)和16-周(仅经历PRS治疗)时间评价MAVYRET的疗效。经历PRS治疗-用MAVYRET治疗受试者共16周中,49%(34/69)有以前含索非布韦方案失败。
14.5未治疗过和经历PRS治疗-成年有CKD 4和5期和慢性HCV感染无肝硬化或有代偿的肝硬化
EXPEDITION-4为一项开放,单-臂,多中心试验在有严重肾受损(CKD 4和5期)有代偿肝疾病(有或无Child-Pugh A肝硬变)评价受试者安全性和疗效。纳入有104例受试者,82%为用血液透析,和分别53%,15%,11%,19%,1%和1%为感染的有HCV基因型1,2,3,4,5和6。 总体而言,19%受试者有代偿的肝硬变和81%的受试者为非-肝硬变;分别58%和42%的受试者为未治疗过和经历PRS治疗。总体SVR12率为98%和无受试者经历病毒学失败。肾受损的存在不影响疗效;试验期间无需剂量调整。.
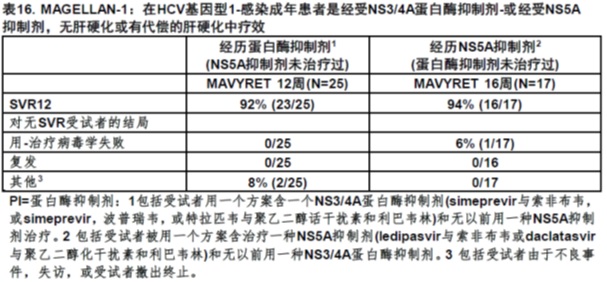
14.6 成年为NS5A抑制剂或NS3/4A-蛋白酶抑制剂(PI)-经历,无肝硬化或有代偿的肝硬化
MAGELLAN-1是一项随机化,多部分,开放试验在141例基因型1-或4-感染的受试者患者含一个NS5A抑制剂和/或NS3/4A蛋白酶抑制剂以前方案失败。部分1(n=50)为一个随机化试验开拓12周的glecaprevir 200 mg和pibrentasvir 80 mg,glecaprevir 300 mg和pibrentasvir 120 mg,有或无利巴韦林(在这些分析仅被包括数据来自glecaprevir 300 mg加pibrentasvir 120 mg无利巴韦林)。部分2(n=91)随机化基因型1-或4-感染的受试者无肝硬化或有代偿的肝硬化至用MAVYRET 12-或16-周的治疗。
在部分1和2的42例基因型1-感染的被治疗受试者,是或仅经受NS5A抑制剂(和被治疗共16周),或仅经历NS3/4A PI(和被治疗共12周),中位年龄为58岁(范围:34至70);40%的受试者为仅经历NS5A治疗和60%为仅经历蛋白酶抑制剂[PI];24%有肝硬变;19%为≥65岁,69%为男性;26%为黑种人;43%有一个机体质量指数≥ 30 kg/m2;67%有基线HCV RNA水平至少1,000,000 IU每mL;79%有亚型1a感染,17%有亚型1b感染和5%有非-1a/1b感染。
由于病毒学失败的较高率和治疗-出现药物耐药性,数据不支持不支持标记为HCV基因型1感染的患者的治疗患者是NS3/4A蛋白酶抑制剂[PI]和经历NS5A抑制剂两者。
16 如何供应/贮存和处置
MAVYRET被发放在一个4-周(每月)或一个8-周纸盒。每个每周纸盒含7次每天天剂量药包[wallets]。每个每月纸盒含有四个每周纸盒。每个8周纸盒含有2个每月纸盒。每个防儿童每天剂量药包含有三个100 mg/40 mg glecaprevir/pibrentasvir片。MAVYRET片是粉色,膜包衣,椭圆形,双凹在一侧凹陷有“NXT”。
NDC号为:
●4-周纸盒:0074-2625-28
●8-周纸盒:0074-2625-56
贮存在或低于30°C(86°F).
17 患者咨询资料
建议患者阅读FDA-批准的患者说明书(患者资料)。
在与HCV和HBV共感染的患者中乙型病毒性肝炎再活化的风险
告知患者在患者共感染有HBV期间或HCV感染的治疗后可能发生HBV再活化。建议患者告诉他们的卫生保健提供者如他们有乙型病毒感染病史[见警告和注意事项(5.1)]。
药物相互作用
告知患者MAVYRET可能与有些药物相互作用;所以,患者应被忠告报告至他们的卫生保健提供者任何处方,非-处方药或草药产品的使用[见禁忌证(4),警告和注意事项(5.2)和药物相互作用(7)]。
给药
建议患者服用MAVYRET推荐剂量(三片)与食物每天1次按指示。告知患者重要的是不要缺失或跳过剂量和服用MAVYRET按医生推荐的时间[见剂量和给药方法(2.2)]。
如一个剂量被缺失和它是:
●从寻常时间低于18小时MAVYRET应被服用 – 建议患者尽可能立即服用剂量和然后在寻常时间服用下一次剂量。
●从MAVYRET应被服用的寻常时间超过18小时– 建议患者不要服用缺失剂量和在寻常时间服用下一次剂量。

