Gilotrif(afatinib)片使用说明书2013年第一版
批准日期: 2013年7月12日;公司: Boehringer Ingelheim Pharmaceuticals Inc.
美国FDA药物评价和研究中心血液学和肿瘤学室主任Richard Pazdur,M.D.说:“今天的批准进一步示范更多了解所患疾病的分子通路可能导致靶向治疗的发展,”“Gilotrif是今年被批准对有其肿瘤有EGFR外显子19缺失或外显子21 L858R取代突变未治疗的转移NSCLC患者第二个药物。” 美国FDA装置和放射卫生中心在体外诊断和放射卫生室主任Alberto Gutierrez,Ph.D.说:“协同诊断测试和药物的批准在肿瘤学是重要发展,因为它们帮助我们对需要它们患者的安全和有效治疗。”
优先审评
http://www.accessdata.fda.gov/drugsatfda_docs/label/2013/201292s000lbl.pdf
处方资料重点
这些重点不包括安全和有效使用GILOTRIF所需所有资料。请参阅GILOTRIF完整处方资料。
GILOTRIF™ (afatinib)片,为口服使用
美国初次批准:2013
适应证和用途
GILOTRIF是一种激酶抑制剂适用为有转移非小细胞肺癌(NSCLC)患者一线治疗其肿瘤有当用FDA批准的测试检出的表皮生长因子受体(EGFR)外显子19缺失或外显子21(L858R)取代突变。(1)
使用限制:尚未在肿瘤有其他EGFR突变患者中确定GILOTRIF的安全性和疗效。 (1)
剂量和给药方法
(1)推荐剂量:40 mg口服,每天1次 (2.2)
(2)指导患者在进餐前至少1小时或后2小时服用GILOTRIF (2.2)
剂型和规格
片:40 mg,30 mg,和20 mg (3)
禁忌证
无(4)
警告和注意事项
(1)腹泻:腹泻可能导致脱水和肾衰。对严重和对抗腹泻药物无反应延长腹泻不给GILOTRIF。 (2.3,5.1)
(2)大疱和剥脱性皮肤疾病:0.15%患者中生严重大疱,起泡,和去角质病变。对威胁生命的皮肤反应终止药物。对严重和延长皮肤反应不给GILOTRIF。 (2.3,5.2)
(3)间质性肺病(ILD):在1.5%患者发生。对肺症状急性发作或恶化不给GILOTRIF。如被诊断ILD终止 GILOTRIF。 (2.3,5.3)
(4)肝毒性:在0.18%患者中发生致命性肝损伤。用定期肝检验监视。对肝检验严重或恶化不给或终止 GILOTRIF。 (2.3,5.4)
(5)角膜炎:在0.8%患者中发生。不给GILOTRIF对角膜炎评价。对确证溃疡性角膜炎不给或终止GILOTRIF。(2.3,5.5)
(6)胚胎胎儿毒性:可致胎儿危害。劝告女性对胎儿潜在危害和使用高效避孕。(5.6)
不良反应
最常见不良反应(≥20%)是腹泻,皮疹/痤疮样皮炎,口腔炎,甲沟炎,干皮肤,食欲减低,瘙痒。(6.1)
为报告怀疑不良反应,联系Boehringer Ingelheim Pharmaceuticals,Inc.电话(800)542-6257或(800) 459-9906 TTY或FDA电话1-800-FDA-1088或www.fda.gov/medwatch。
药物相互作用
P-gp抑制剂的共同给药可能增加afatinib暴露。如不能耐受每天减低GILOTRIF 10 mg。慢性Pgp诱导剂口服的共同给药可能减低afatinib暴露。当耐受时每天增加GILOTRIF 10 mg。(2.3,7)
在特殊人群中使用
哺乳母亲:终止药物或哺乳。(8.3)
完整处方资料
1 适应证和用途
GILOTRIF is适用为有转移非小细胞肺癌(NSCLC)患者的一线治疗,当用FDA批准的测试检出患者肿瘤有表皮生长因子受体(EGFR)外显子19缺失或外显子21(L858R)取代突变[见临床研究 (14)]。
使用限制:尚未确定其肿瘤有其他EGFR突变患者GILOTRIF的安全性和疗效[见临床研究 (14)]。
2 剂量和给药方法
2.1 患者选择
选择患者为用GILOTRIF转移NSCLC一线治疗。根据在肿瘤标本中存在EGFR外显子19缺失或外显子21 (L858R)取代突变 [见适应证和用途(1)和临床研究(14.1)]。对FDA-批准的检验检测NSCLC中EGFR突变信息在下列网址:http://www.fda.gov/CompanionDiagnostics。
2.2 推荐剂量
GILOTRIF的推荐剂量是40 mg口服每天1次直至疾病进展或患者无较长耐受。在餐前至少1小时或餐后2小时服用GILOTRIF。
在下次给药12小时内不要服用丢失剂量。
2.3 剂量修饰
对任何药物相关不良反应不给GILOTRIF:
●NCI CTCAE* 3级或更高
●当服用抗-腹泻药物2级或更高腹泻持续连续2或更多天 [见警告和注意事项(5.1)]
●延长2级皮肤反应(持续长于7天)或不能耐受 [见警告和注意事项(5.2)]
●2级或更高肾功能不全
*美国国家癌症研究所对不良事件常用名词标准,v 3.0
当不良反应完全解决,返回基线,或改善至1级恢复治疗。再开始GILOTRIF在减低剂量,即,小于发生不良反应剂量每天10 mg。
对以下永远 终止GILOTRIF:
● 威胁生命大疱,起泡,或剥脱性皮肤病变[见警告和注意事项(5.2)]
● 确证间质性肺病(ILD)[见警告和注意事项(5.3)]
● 严重药物诱导肝受损[见警告和注意事项(5.4)]
● 持久性溃疡性角膜炎[见警告和注意事项(5.5)]
● 症状性左室功能障碍。
● 在剂量每天20 mg发生严重或不能耐受的不良反应
P-gp抑制剂
对需要用P-糖蛋白(P-gp)抑制剂治疗患者,如不能耐受减低每天GILOTRIF 剂量10 mg。终止P-gp抑制剂当耐受时恢复以前剂量[见药物相互作用(7)和临床药理学(12.3)]。
P-gp诱导剂
对需要用一种P-gp诱导剂慢性治疗患者,如能耐受增加每天GILOTRIF 剂量10 mg。终止P-gp诱导剂后2至3天恢复以前剂量[见药物相互作用(7)和临床药理学(12.3)]。
3 剂型和规格
可以得到如下GILOTRIF:40 mg片:浅蓝色,薄膜包衣,圆,双凸形,斜缘片在一侧凹陷有“T40"和在另一侧Boehringer Ingelheim公司符号。
30 mg片:暗蓝色,薄膜包衣,圆,双凸形,斜缘片在一侧凹陷有“T30”和在另一侧Boehringer Ingelheim公司符号。
20 mg片:白色至淡黄色,薄膜包衣,圆,双凸形,斜缘片在一侧凹陷有“T20”和在另一侧Boehringer Ingelheim公司符号。
4 禁忌证
无。
5 警告和注意事项
5.1 腹泻
腹泻曾导致脱水有或无肾受损;这些有些病例是致命性。在研究1中,在96%的用GILOTRIF治疗患者(n=229)发生腹泻,其中严重程度3级为15%和发生在头6周内[见不良反应(6.1)]。6.1%用GILOTRIF治疗患者腹泻的后果是肾受损,其中3例(1.3%)为3级。
对发生延长2级腹泻持续长于48小时或更长或等同3级腹泻患者,不给GILOTRIF直至腹泻 解决至1级或更低,和用适当剂量减低恢复GILOTRIF[见剂量和给药方法(2.3)]。在腹泻发作时提供患者用一种抗腹泻药(如,洛哌丁胺[loperamide])为自身给药和指导患者继续抗腹泻治疗直至稀便停止12小时。
5.2 大疱和剥脱性皮肤疾病
跨越临床试验3865例接受GILOTRIF患者,3级皮肤反应特征为大疱,起泡,和去角质病变发生6例(0.15%)[见不良反应(6.1)]。在研究1中,皮肤反应的总发生率皮疹,红斑,和痤疮皮疹组成为90%,而3级皮肤反应的发生率为16%。此外,1-3级掌跖红肿疼痛综合征的发生率为7%。在发生威胁生命大疱,起泡,或去角质病变患者中终止GILOTRIF[见剂量和给药方法(2.3)]。 对发生延长的2级皮肤不良反应持续7天以上,不能耐受的2级,或3级皮肤反应患者,不给GILOTRIF 直至不良反应解决至1级或更低和以适当剂量减低恢复GILOTRIF[见剂量和给药方法(2.3)]。
5.3 间质性肺病(ILD)
跨越临床试验3865例接受GILOTRIF患者1.5%发生ILD或ILD-样不良反应(如,肺浸润,肺炎,急性呼吸窘迫综合征,或肺泡过敏);其中0.4%是致命性。在亚裔种族患者(2.1%)当与非-亚裔(1.2%)比较ILD的发生率似乎较高。在研究1中,在1% GILOTRIF-治疗患者中≥3级ILD的发生率为1.3%和导致死亡。
有怀疑的ILD患者评价期间不给GILOTRIF,而有确证ILD患者中终止GILOTRIF[见剂量和给药方法(2.3)]。
5.4 肝毒性
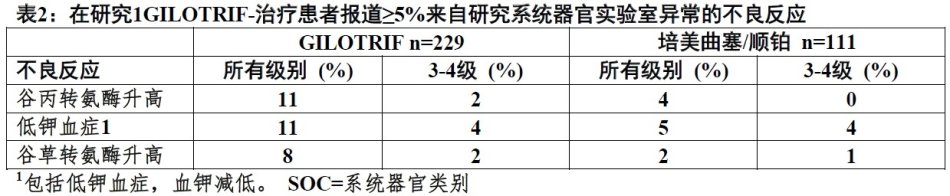
跨越临床试验在3865例接受GILOTRIF患者,10.1%有肝检验异常,其中7例(0.18%)为致命性。 在研究1中,用GILOTRIF治疗患者任何级别肝检验异常发生17.5%。
患者用GILOTRIF治疗期间得到定期肝检验。发生肝功能恶化患者不给GILOTRIF[见剂量和给药方法(2.3)]。在用GILOTRIF发生严重肝损伤患者应终止治疗。
5.5 角膜炎
跨越临床试验用GILOTRIF治疗3865例患者中0.8%患者发生角膜炎,特征为急性眼炎症或恶化,流泪,光敏感,视力模糊,眼痛,和/或红眼。在研究1中报道5 (2.2%)角膜炎患者,3级1 (0.4%)。怀疑角膜炎患者评价期间不给GILOTRIF,而如确证溃疡性角膜炎,用中断或终止GILOTRIF治疗[见剂量和给药方法(2.3)]。如诊断角膜炎应仔细考虑继续治疗获益和风险。有角膜炎,溃疡性角膜炎,或严重干眼史患者中应谨慎使用GILOTRIF[见不良反应(6.1)]。对角膜炎和溃疡使用隐形眼镜也是风险。
5.6 胚胎胎儿毒性
根据其作用机制,当给予妊娠妇女GILOTRIF可致胎儿危害。Afatinib是胚胎胎儿毒性和,在动物中有母体毒性,在兔中在剂量5 mg/kg (约为人推荐剂量每天40 mg人暴露0.2倍)或更大导致晚妊娠阶段流产。如妊娠时使用此药,或当服用此药时患者成为妊娠,应忠告患者对胎儿潜在危害[见在特殊人群中使用(8.1)]。
忠告有生殖潜力女性治疗期间和末次给予GILOTRIF后至少2周使用高效避孕。忠告患者如她们当服用GILOTRIF成为妊娠或如怀疑妊娠联系她们的卫生保健提供者[见在特殊人群中使用(8.1和8.6)]。
6 不良反应
在说明书其他节更详细讨论以下不良反应:
●腹泻[见警告和注意事项(5.1)]
●大疱和剥脱性皮肤疾病[见警告和注意事项(5.2)]
●间质性肺病[见警告和注意事项(5.3)]
●肝毒性[见警告和注意事项(5.4)]
●角膜炎[见警告和注意事项(5.5)]
6.1 临床试验经验
因为临床试验是在广泛不同情况下进行的,临床试验观察到不良反应率不能与另一种药临床试验发生率直接比较而且可能不反映实践中观察到的发生率。
GILOTRIF的安全性评价是根据来自3800例以上患者数据,包括2135例NSCLC患者接受GILOTRIF单药治疗在推荐剂量或以上。
对照研究
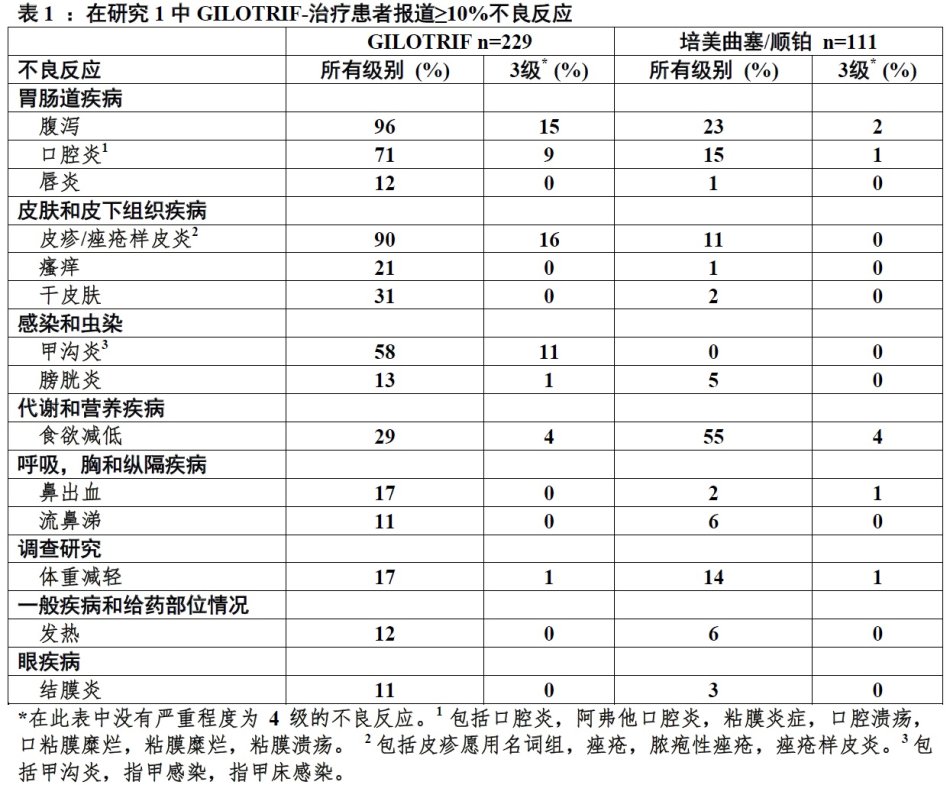
下面表1和2数据反映有EGFR突变-阳性,转移,非鳞状,NSCLC纳入一项随机化,多中心,开放试验(研究1)229例天然EGFR-TKI GILOTRIF-治疗患者的暴露。患者每天接受GILOTRIF 40 mg直至记录疾病进展或不能耐受治疗。总共111例患者用培美曲塞/顺铂治疗。患者用培美曲塞500 mg/m²30分钟后接着顺铂75 mg/m²每三周1次治疗共最大六个 治疗疗程。
对用GILOTRIF治疗患者中位暴露为11.0个月和对用培美曲塞/顺铂治疗患者3.4个月。总体试验人群中位年龄61岁;GILOTRIF组61%患者和培美曲塞/顺铂组60%患者年龄小于65岁。用GILOTRIF患者64%和培美曲塞/顺铂患者67%为女性。三分之二以上患者来自亚裔(GILOTRIF 70%;培美曲塞/顺铂72%)。
用GILOTRIF治疗患者报道严重不良反应29%。用GILOTRIF治疗患者报道最频严重不良反应是腹泻(6.6%);呕吐(4.8%),和呼吸困难,疲乏,和低钾血症(各1.7%)。在研究1中GILOTRIF-治疗患者致命性不良反应包括肺毒性/ILD-样不良反应(1.3%),脓血症(0.43%),和肺炎 (0.43%)。
GILOTRIF-治疗患者57%由于不良反应需要减低剂量。用GILOTRIF治疗患者最频不良反应导致剂量减低是腹泻(20%),皮疹/痤疮(19%),甲沟炎(14%),和口腔炎(10%)。
为不良反应GILOTRIF-治疗患者14.0%终止治疗。GILOTRIF-治疗患者导致终止最频不良反应是腹泻(1.3%),ILD (0.9%),和甲沟炎(0.9%)。
GILOTRIF的临床试验排除有左室射血分数(LVEF)异常患者,即,低于机构正常的低限。在研究1中,所有患者在筛选时和其后每9周在GILOTRIF-治疗组和在培美曲塞/顺铂组当需要时评价LVEF。与化疗-治疗患者比较(0.9%;n=1),更多GILOTRIF-治疗患者(2.2%;n=5)经受心功能不全(被定义为舒张功能障碍,左室功能障碍,或心室扩展;所有< 3级)。
7 药物相互作用
P-糖蛋白(P-gp)抑制剂和诱导剂的影响
在给予GILOTRIF前1小时口服给予一种P-gp抑制剂(利托那韦[ritonavir]在200 mg每天2次)增加对afatinib全身暴露48%。当利托那韦是同时给予或GILOTRIF后6小时afatinib暴露没有变化。与GILOTRIF同时服用P-gp抑制剂(包括但不限于利托那韦,环孢霉素A[cyclosporine A],酮康唑[ketoconazole],伊曲康唑[itraconazole],红霉素[erythromycin],维拉帕米[verapamil],奎尼丁[quinidine],他克莫司[tacrolimus],奈非那韦[nelfinavir],沙奎那韦[saquinavir],和胺碘酮[amiodarone])可能增加对afatinib暴露[见剂量和给药方法(2.3)和临床药理学(12.3)]。
与口服剂量P-gp诱导剂共同给药(利福平[rifampicin]600 mg每天1次共7天)减低对afatinib暴露 34%。GILOTRIF同时用P-gp诱导剂(包括但不限于利福平,卡马西平[carbamazepine],苯妥英[phenytoin],苯巴比妥[phenobarbital],和圣约翰草[St. John’s wort])可能减低对afatinib暴露[见剂量和给药方法(2.3)和临床药理学(12.3)]。
8 在特殊人群中使用
8.1 妊娠
妊娠类别D
风险总结
根据其作用机制,当给予妊娠妇女GILOTRIF可致胎儿危害。Afatinib是胚胎毒性和,在动物中有母体毒性,在兔中在剂量5 mg/kg(按AUC约推荐人剂量每天40 mg暴露的0.2倍)或更大在妊娠晚期导致流产。如此药在妊娠期间使用,或服用此药时患者成为妊娠,应忠告患者对胎儿潜在危害[见警告和注意事项(5.6)]。
动物数据
在器官形成期时给予妊娠兔Afatinib在剂量5 mg/kg (按照AUC约推荐人剂量每天40 mg暴露的0.2倍)或更大引起植入后丢失增加和,凋亡显示母体毒性,在妊娠晚期流产。在相同研究中,在高剂量水平10 mg/kg(按AUC暴露约人推荐剂量每天40 mg的0.7倍)有减低胎儿体重,和增加 矮小畜[runts]的发生率,以及内脏和皮肤变异。在大鼠中一项胚胎胎儿发育研究,有不完全或延迟骨化头颅改变组成和减低胎儿体重在剂量16 mg/kg(约推荐人剂量每天40 mg暴露两倍)。
8.3 哺乳母亲
不知道afatinib是否存在在人乳汁中,给药后1至6小时发现Afatinib存在于哺乳大鼠乳汁中在浓度80-150倍较高与血浆浓度。因为许多药物存在于人乳汁和因为在哺乳婴儿来自GILOTRIF潜在严重不良反应,应做出决策是否终止哺乳或终止药物,考虑药物对母亲的重要性。
8.4 儿童使用
尚未在儿童患者中确定GILOTRIF的安全性和有效性。
8.5 老年人使用
在GILOTRIF的临床研究3865例患者中,32%患者是65岁和以上,而7%是75岁和以上。在65岁和以上患者和较年轻患者间未观察到安全性的总体差别。在研究1中,345例39%患者是65岁或以上和4%是75岁或以上。未观察到65 岁和以上患者和较年轻患者间有效性总体差别。
8.6 生殖潜力女性和男性
避孕
女性
与患者商量妊娠计划和预防。忠告有生殖潜力女性患者用GILOTRIF治疗期间和GILOTRIF末次给药后至少2周使用高效避孕。忠告患者当服用GILOTRIF时如她们成为妊娠或怀疑妊娠联系其卫生保健提供者[见在特殊人群中使用(8.1)]。
8.7 肾受损
尚未在有严重肾功能受损(肌酐清除率[CLcr] <30 mL/min)患者中研究GILOTRIF 。在有轻度(CLcr 60-89 mL/min)肾受损患者不考虑需要调整GILOTRIF起始剂量。有中度(CLcr 30-59 mL/min)至严重(CLcr< 30 mL/min)肾受损密切监视患者和如不能耐受调整GILOTRIF剂量[见临床药理学(12.3)]。
8.8 肝受损
尚未在严重(Child Pugh C)肝受损患者研究GILOTRIF。在有轻度(Child Pugh A)或中度(Child Pugh B)肝受损患者中不考虑需要调整GILOTRIF的起始剂量。严密监视患者有严重肝受损和如不能耐受调整 GILOTRIF剂量[见临床药理学(12.3)]。
10 药物过量
报道药物过量在2例健康青少年中个摄入360 mg的GILOTRIF(作为混合药物摄入的部分)导致恶心,呕吐,乏力,眩晕,头痛,腹痛,和淀粉酶升高(正常上限[ULN]<1.5倍)。两例受试者都恢复。
11 一般描述
GILOTRIF片含afatinib,一种酪氨酸激酶抑制剂是一个4-anilinoquinazoline。Afatinib以二马来酸酯盐存在,化学名2-butenamide,N-[4-[(3-chloro-4-fluorophenyl)amino]7-[[(3S)-tetrahydro-3-furanyl]oxy]-6-quinazolinyl]-4-(dimethylamino)-,(2E)-,(2Z)-2-butenedioate (1:2)。其结构式为;
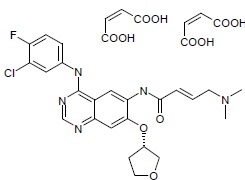
Afatinib二马来酸酯盐是一种白色至棕黄色份,水溶性和吸湿性,经验式C32H33ClFN5O11,和分子量718.1 g/mol。
为口服给药GILOTRIF片可得到40 mg,30 mg,或20 mg afatinib(分别等同于59.12 mg,44.34 mg,或29.56 mg afatinib二马来酸酯盐)。GILOTRIF的无活性成分如下:片芯:一水乳糖,微晶纤维素,交联聚乙烯吡咯烷酮,胶态二氧化硅,硬脂酸镁。壳:羟丙甲纤维素,聚乙二醇,二氧化钛,滑石粉,聚山梨醇80,FD&C蓝No. 2 (仅40 mg和30 mg片)。
12 临床药理学
12.1 作用机制
Afatinib与EGFR(ErbB1),HER2 (ErbB2),和HER4 ErbB4)的激酶结构域共价结合和不可逆地抑制酪氨酸激酶自身磷酸化,导致ErbB信号的下调。
Afatinib显示自身磷酸化的抑制作用和在体外表达野生型EGFR细胞株的增殖或表达选择性EGFR外显子19缺失突变或外显子21 L858R突变,包括在患者中在可到达的afatinib浓度时,至少暂时,某些有一种次发T790M突变。此外,在体外afatinib抑制过表达HER2细胞株的增殖。
在植入肿瘤或过表达野生型 EGFR或HER2或在一种EGFR L858R/T790M双突变体模型裸鼠中用afatinib治疗导致肿瘤生长的抑制。
12.2 药效动力学
心脏电生理学
在有复发或难治性实体肿瘤患者一项开放,单组研究中评价多剂量GILOTRIF(50 mg 每天1次)对QTc间期的影响。在研究中未检出平均QTc间期(即,>20 ms)大变化。
12.3 药代动力学
吸收和分布
GILOTRIF片口服给药后,Afatinib血浆浓度达峰(Tmax)是2至5小时。在20至50 mg范围内最大浓度(Cmax)和从零时至无限时时间浓度曲线下面积(AUC0-∞)值增加略微大于正比例。20 mg GILOTRIF片当与一个口服溶液比较为几何均数相对生物利用度为92%。在体外afatinib与人血浆蛋白的结合是约95%。
一个高脂肪餐相对于空腹条件降低Cmax 50%和AUC0-∞ 39%[见剂量和给药方法(2.2)]。
代谢和消除
与蛋白共价加合物是afatinib的主要循环代谢物和afatinib的酶学代谢小。
在人中,单次口服剂量[14C]-标记的afatinib溶液后afatinib的排泄主要通过粪(85%)在尿中回收 4%。母体化合物占回收剂量的88%。
在癌症患者中重复给药后Afatinib的消除半衰期为37小时。重复给予GILOTRIF的8天内达到稳态血浆浓度导致对AUC蓄积2.8-倍和对Cmax蓄积2.1-倍。
特殊人群
肾受损:在有轻度患者(CLcr 60-89 mL/min)和中度(CLcr 30-59 mL/min)肾受损与有正常肾功能(CLcr ≥90 mL/min)患者比较中位谷afatinib血浆浓度较高27%和85%。尚未在有严重受损肾功能(CLcr< 30 mL/min)患者中研究GILOTRIF[见在特殊人群中使用(8.7)]。
肝受损:Afatinib主要通过胆汁/粪排泄被消除。单剂量GILOTRIF后,轻度(Child Pugh A)或中度(Child Pugh B)肝受损对afatinib暴露没有影响。尚未研究受试者有严重(Child Pugh C)肝功能不全[见在特殊人群中使用(8.8)]。
体重,性别,年龄,和种族:根据群体药代动力学分析,体重,性别,年龄,和种族对afatinib的暴露没有临床上重要影响。
药物相互作用
P-gp抑制剂和诱导剂对Afatinib的影响:在健康受试者单独服用40 mg GILOTRIF与在GILOTRIF给予后6小时时利托那韦(200 mg每天2次共3天)共同给药后比较评价利托那韦给药时间相对于单次口服剂量GILOTRIF的影响。当与利托那韦共同给药时,Afatinib的AUC0-∞和Cmax相对生物利用度为119%和104% 而当服用GILOTRIF后6小时给予利托那韦为111%和105%。在另外一项研究,当20 mg单剂量GILOTRIF前1小时给予利托那韦(200 mg每天2次共3天),对AUC0-∞对afatinib暴露 增加48%和对Cmax为39%[见药物相互作用(7)]。
用一种强P-gp诱导剂,利福平(600 mg每天1次共7天)预-治疗减低对afatinib血浆暴露 34%(AUC0-∞)和22% (Cmax)[见药物相互作用(7)]。
P-糖蛋白(P-gp):根据在体外数据,afatinib是P-gp的某种底物和某种抑制剂。
乳腺癌耐药蛋白(BCRP):根据在体外数据,afatinib是转运蛋白BCRP的底物和一种抑制剂。
CYP450酶诱导剂和抑制剂对Afatinib的影响:在体外数据表明药物-药物相互作用用GILOTRIF由于CYP450酶被同时用药抑制或抑制作用是不可能。通过CYP450-依赖反应形成的代谢物是在夹心饼干培养人肝细胞总代谢更新的约9%。在人中,对afatinib的代谢酶-催化代谢反应作用可忽略不计。afatinib剂量的约2%被FMO3代谢;未检测到CYP3A4-依赖N-去甲基作用。
Afatinib对CYP450酶的影响:在原代人肝细胞培养中Afatinib不是CYP450酶(CYP1A2,2B6,2C8,2C9,2C19,和3A4)抑制剂或诱导剂。因此,afatinib不可能影响CYP450酶底物的其他药物的代谢。
13 非临床毒理学
13.1 癌发生,突变发生,生育能力受损
尚未用afatinib进行致癌性研究。
在单一检测株细菌(Ames)致突变试验观察到对afatinib的边缘反应。在体外染色体畸变检验在非-细胞毒浓度以及在体内骨髓微核试验,体内Comet试验,和在Muta™ 小鼠体内4-周口服突变研究均确定无致突变或遗传毒性潜能。
在一项专门生育能力研究,雄性和雌性大鼠每天口服给予接受afatinib剂量4,6,或8 mg/kg。在雄性在剂量mg/kg(AUC约等于暴露患者在推荐人剂量每天40 mg)或更大,低或无精子计数的发生率增加,虽然总体生育能力未受影响;精子计数减低被睾丸中凋亡增加发现和精囊和e一般毒理学研究前列腺萎缩。在雌性中在高剂量8 mg/kg (约为推荐人剂量每天40 mg患者AUC暴露0.63倍),黄体数轻度减低与由于早期再吸收植入后丢失轻度增加。在一项4-周一般毒理学研究,雌性大鼠在所有剂量水平有卵巢重量减低;在2周恢复期结束时器官重量没有完全恢复。
14 临床研究
非小细胞肺癌(NSCLC)
研究1
在345患者有EGFR突变-阳性,转移(阶段IV和阶段IIIb有胸膜和/或心包积液按美国癌症联合委员会[AJCC,第六版])分类NSCLC的一项随机化,多中心,开放试验(研究1)的一线治疗确定GILOTRIF的疗效和安全性。患者被(2:1)随机化接受GILOTRIF 40 mg口服每天1次(n=230)或直至6个疗程的培美曲塞/顺铂 (n=115)。按照EGFR突变状态(外显子19缺失相比外显子21 L858R相比其他)和种族(亚裔相比非亚裔)随机化分层。主要疗效结局是由独立审评委员会(IRC)评估的无进展生存(PFS)。其他疗效结局包括客观反应率(ORR)和总生存(OS)。对筛选和纳入患者用一个临床试验分析(CTA)前瞻性测定EGFR突变状态。来自264例患者(178 随机化至GILOTRIF和86例患者随机化至化疗) 肿瘤样品被用协同诊断 therascreen® EGFR RGQ PCR药盒,它被FDA-批准为选择患者对GILOTRIF 治疗回顾性测试。
随机化患者中,65%是女性,中位年龄为61岁,基线ECOG体能状态状态为0 (39%)或1 (61%),26% 是高加索人和72%是亚裔。患者的大多数有肿瘤样品有按CTA分类的一种EGFR突变 为或外显子19缺失(49%)或外显子21 L858R取代(40%),而其余11% 有其他突变。
通过IRC确定患者随机化至GILOTRIF与随机化至化疗患者比较PFS有统计显著改善。见表3和图1。在进行中期分析时,在84%计划事件时,对最终分析治疗组间总生存无统计意义差别。
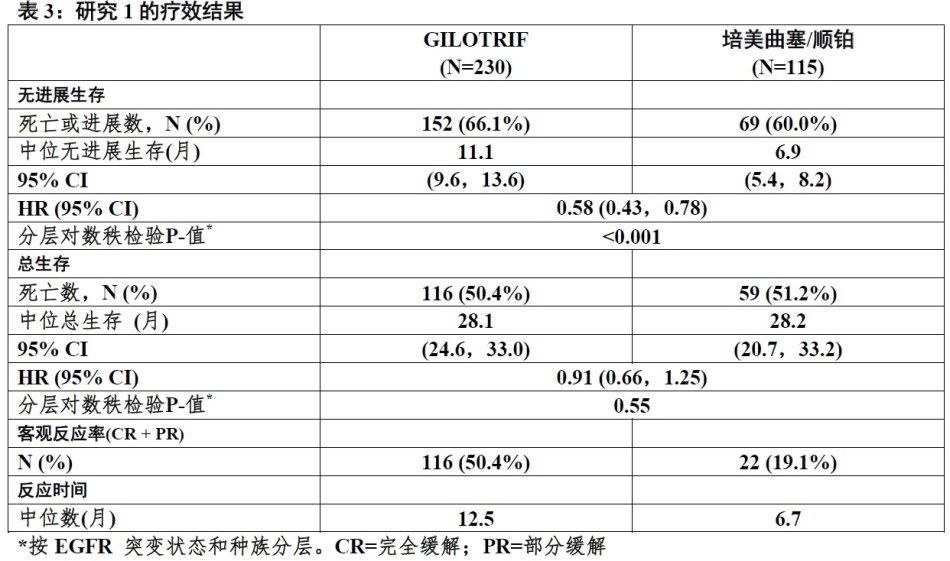
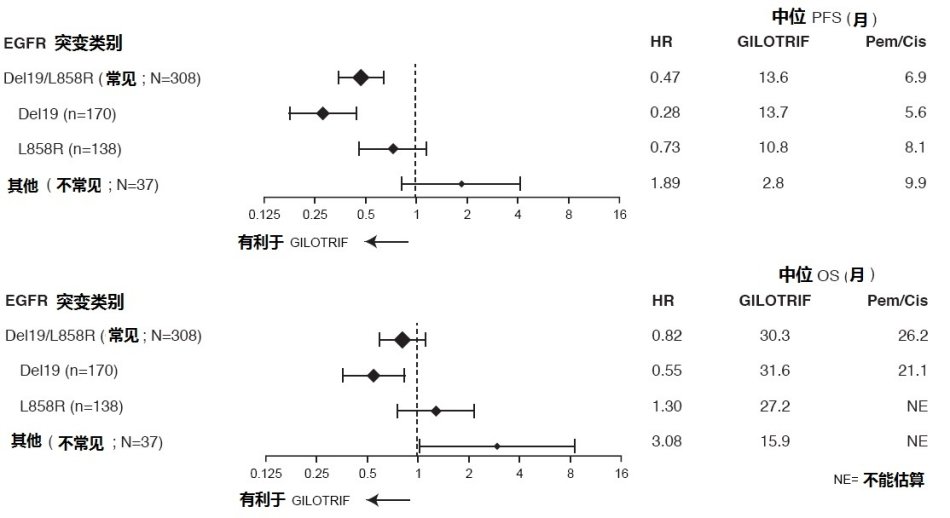
图1 由独立审评按治疗组对PFS 的Kaplan-Meier 曲线
根据EGFR突变状态的分层因子(Del19,L858R,其他)和突变分类(常见[Del19,L858R]相比不常见[其他])进行亚组分析。见图2。
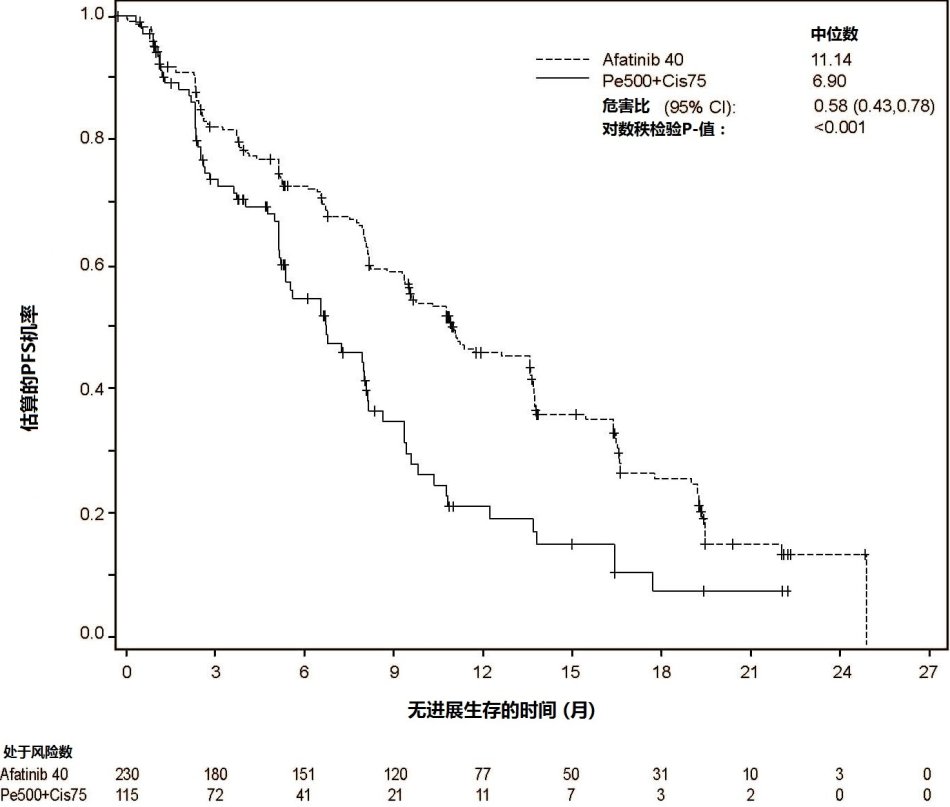
图2对常见(Del19,L858R)和非常见(其他)EGFR突变类别PFS和OS的森林图[Forest Plot]
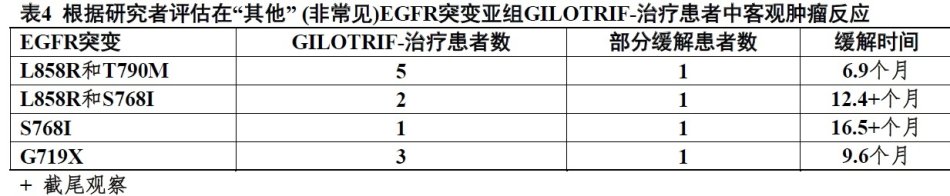
在“其他”(非常见) EGFR突变亚组中有26例GILOTRIF-治疗患者有9例独特突变型式。None of这些26例患者没有一例达到完全缓解,而四例达到部分缓解(见下表4)。在有以下突变GILOTRIF-治疗患者未见反应:单独T790M(n=2),缺失19和T790M(n=3),G719X和T790M (n=1),外显子20插入(n=6),和单独L861Q (n=3。在“其他”非常见EGFR 突变亚组有11例化疗-治疗患者;这些其中,4例(36%)达到部分缓解。
16 如何供应/贮存和处置
GILOTRIF片可得到如下:40 mg:浅蓝色,薄膜包衣,圆,双凸形,斜缘片在一侧凹陷有“T40”和在另一侧Boehringer Ingelheim公司符号。
30片瓶使用单元 NDC:0597-0138-30
30 mg:暗蓝色,薄膜包衣,圆,双凸形,斜缘片在一侧凹陷有“T30”和在另一侧Boehringer Ingelheim公司符号。
30片瓶使用单元 NDC:0597-0137-30
20 mg:白色至淡黄色,薄膜包衣,圆,双凸形,斜缘片在一侧凹陷有“T20”和在另一侧Boehringer Ingelheim公司符号。
30片瓶使用单元 NDC:0597-0141-30
贮存
贮存在25°C(77°F);外出允许至15°-30°C(59°-86°F)[见USP控制室温]。发放药物在原始容器内避免暴露至高湿度和光。
17 患者咨询资料
见FDA-批准的患者使用说明书(患者资料)
● 腹泻
忠告患者接近所有l患者接受GILOTRIF发生腹泻。告知患者腹泻如不治疗可能导致脱水和肾受损。忠告患者如发生腹泻告知其医生和对严重或持续腹泻立即寻求医学关注[见警告和注意事项(5.1)和不良反应(6.1)]。
● 大疱和剥脱性皮肤疾病
忠告患者穿保护衣服减少阳光暴露和服GILOTRIF时用防晒霜[见警告和注意事项(5.2)]。
● 间质性肺病
忠告患者立即报告任何新或恶化肺症状,或任何以下症状的组合:呼吸困难或气短,咳嗽,发热[见警告和注意事项(5.3)]。
● 肝毒性
忠告患者他们将需要定期进行肝功能监视。忠告患者立即报告肝问题症状(如,皮肤或眼白变黄,尿暗色或棕色(茶色),胃右侧疼痛,出血或比正常更易瘀伤,昏睡)[见警告和注意事项(5.4)]。
● 角膜炎
忠告患者立即报告任何眼问题(如,眼痛,肿胀,发红,视力模糊,或其他视力变化)[见警告和注意事项(5.5)]。
● 左室功能不全
忠告患者对任何以下立即联系卫生保健专业人员:新发作或恶化气短或不能耐受活动,咳嗽,疲乏,关节腿肿胀,心悸,或体重突然增量[见剂量和给药方法(2.3)和不良反应(6.1)]。
●对服用GILOTRIF指导
忠告患者空胃服用GILOTRIF饭后至少1小时前或2小时后[见剂量和给药方法(2.2)]。忠告患者在下次给药12小时内不要服用丢失给药。
● 胚胎胎儿毒性
与患者商量妊娠计划和预防。忠告有生殖能力女性治疗期间,和末次给予GILOTRIF后至少2周使用高效避孕[见警告和注意事项(5.6)和在特殊人群中使用(8.1)]。
● 哺乳母亲
忠告患者服用GILOTRIF时终止哺乳[见在特殊人群中使用(8.3)]。

