泰克布TYKERB(拉帕替尼[lapatinib])片使用说明书2010年1月修改版
公司:史克必成(SMITHKLINE BEECHAM)
修改说明书史:01/29/2010 修改说明书;01/29/2010修改说明书;01/29/2010 新或修改适应证;07/07/2008 修改说明书;08/20/2007 修改说明书;4/27/2007修改说明书;03/13/2007批准说明书
处方资料重点
这些重点不包括安全和有效使用泰克布的所有资料。请参阅下文见泰克布完整处方资料。 美国初始批准:2007 优先审评

-最近重要修改
适应证和用途。(1) 01/29/2010
剂量和给药方法。(2) 01/29/2010
禁忌证。(4) 01/29/2010
适应证和用途
泰克布,一种激酶抑制剂,适用于与下述联用:(1)
(1)卡培他滨,为晚期或转移乳腺癌其肿瘤过表达HER2和已接受既往治疗包括一种蒽环类药物,一种紫杉烷,和曲妥珠单抗患者的治疗。
(2)来曲唑为激素受体阳性转移乳腺癌过表达HER2受体适用激素治疗绝经后妇女的治疗。 为转移乳腺癌的治疗未曾比较泰克布与一种芳香化酶抑制剂联用与含曲妥珠单抗化疗方案。
剂量和给药方法
为晚期或转移乳腺癌泰克布的推荐剂量是1,250 mg(5片)在第1-21天连续口服给药每天1次(口服给药2剂间隔约12小时)与卡培他滨2,000 mg/平方米/天联用,一个重复21天疗程中第1-14天。(2.1)
为激素受体阳性, HER2阳性转移乳腺癌,泰克布的推荐剂量是1500 mg(6片)连续口服给药每天1次与来曲唑联用。当泰克布与来曲唑共同给药时,来曲唑的推荐剂量是2.5 mg每天1次。(2.1)
(1)泰克布应在进餐前至少1小时或后1小时服用。但是,卡培他滨应与食物或食物后30分钟内服用(2.1)。 (2)泰克布应每天1次服用。泰克布的每天剂量不要分服。(2.1, 12.3)
(3)为心脏和其它毒性,严重肝受损,和CYP3A4药物相互作用调整剂量。(2.2)
剂型和规格
250 mg片(3)
禁忌证
已知对本品或其任何组分严重超敏性(如,过敏反应)。(4)
警告和注意事项
(1)曾报道左心室射血分数减低。泰克布开始前证实正常LVEF和治疗期间继续评价。(5.1) (2)拉帕替尼曾伴随肝毒性。治疗开始前监查肝功能试验,和当治疗期间临床指示时每4至6周。如患者经受肝功能试验严重变化,终止和不要重新开始泰克布。(5.2)
(3)有严重肝受损患者应考虑减低剂量。(2.2, 5.3, 8.7)
(4)治疗期间曾报道腹泻,包括严重腹泻。如严重用抗-腹泻药处理,和补充液体和电解质。(5.4) (5)拉帕替尼曾伴随间质性肺疾病和肺炎。如患者经受严重肺症状终止泰克布。(5.5)
(6)在某些患者中拉帕替尼可能延长QT间期。考虑监查ECG和电解质。(5.6, 12.6) (7)当给予妊娠妇女可能发生胎儿损害。建议服用泰克布妇女不要成为妊娠。(5.7)
不良反应
用泰克布加卡培他滨治疗期间最常见(>20%)不良反应是腹泻,掌足红肿疼痛,恶心,皮疹,呕吐,和疲劳。用泰克布加来曲唑治疗期间最常见(20%)不良反应是腹泻,皮疹,恶心,和疲劳。 (6.1)
为报告怀疑不良反应联系GlaxoSmithKline公司电话1-888-825-5249或FDA电话1-800-FDA-1088或www.fda.gov/medwatch。
药物相互作用
(1)泰克布很可能增加对同时给予被CYP3A4或CYP2C8代谢药物的暴露。 (7.1)
(2)避免强CYP3A4抑制剂。如不可避免,同时给予强CYP3A4抑制剂患者中.考虑减低泰克布剂量。(2.2, 7.2) (3)避免强CYP3A4诱导剂。如不可避免,同时给予强CYP3A4诱导剂患者中考虑逐渐增加泰克布剂量。(2.2, 7.2)
完整处方资料
黑框警告
![]()
1 适应证和用途
泰克布适用于与下述联用:
(1)卡培他滨[capecitabine]为晚期或转移乳腺癌其肿瘤过表达HER2和既往已接受包括一种蒽环类药物,一种紫杉烷,和曲妥珠单抗[trastuzumab]治疗的患者治疗。
(2)来曲唑[letrozole]为过表达HER2受体适用激素治疗的激素受体阳性转移乳腺癌绝经后妇女的治疗。
未曾为转移乳腺癌的治疗比较泰克布与一种芳香化酶抑制剂联用与含曲妥珠单抗化疗方案。
2 剂量和给药方法
2.1 推荐给药
HER2阳性转移乳腺癌:泰克布的推荐剂量是1,250 mg在第1-21天连续口服给药每天1次与卡培他滨2,000 mg/平方米/天联用一个重复21天疗程中第1-14天(口服给药2剂间隔约12小时)。泰克布应在进餐前至少1小时或后1小时服用。泰克布的剂量应每天 1次(5片1次给予全部);建议每日剂量不要分服[见临床药理学(12.3)]。卡培他滨应与食物或食物后30分钟内,服用如丢失1日剂量,患者下一天剂 量不应加倍。治疗应继续直至疾病进展或发生不可接受的毒性。
激 素受体阳性,HER2阳性转移乳腺癌:泰克布的推荐剂量是1,500 mg口服给药每天1次连续与来曲唑联用。当与泰克布共同给药时,来曲唑的推荐剂量是2.5 mg每天1次。泰克布应在进餐前至少1小时或后1小时服用。泰克布的剂量应每天1次(6片1次给予全部);建议每日剂量不要分服[见临床药理学 (12.3)]。
2.2 调整剂量指导原则
心脏事件:按美国癌症研究所不良反应常用名词标准(NCI CTCAE)患者有左心室射血分数(LVEF)是2级或更高和患者有LVEF减低低于机构的正常下限时应终止泰克布[见警告和注意事项(5.1)和不良反 应(6.1)]。如LVEF恢复正常和患者是无症状,泰克布与卡培他滨联用可能在减低剂量 (1,000 mg/天)而与来曲唑联用可能在减低剂量1,250 mg/天,最少2周后再次开始。
肝受损:有严重肝受损患者(Child-Pugh Class C)应减低其泰克布剂量。(HER2阳性转移乳腺癌适应证)剂量从1,250 mg/天减低至750 mg/天或(激素受体阳性,HER2阳性乳腺癌适应证)从1,500 mg/天减低至1,000 mg/天。应考虑在有严重肝受损患者预计调整曲线下面积(AUC)至正常范围。但是,有严重肝受损患者中用这种调整剂量没有临床资料。.
同时强CYP3A4抑制剂:应避免同时使用强CYP3A4抑制剂(如,酮康唑[ketoconazole],伊曲康唑 [itraconazole],克拉霉素[clarithromycin],阿扎那韦[atazanavir],印地那韦[indinavir],萘法唑 酮[nefazodone],那非那韦[nelfinavir],利托那韦[ritonavir],沙奎那韦[saquinavir],泰利霉素 [telithromycin],伏立康唑[voriconazole])。 葡萄柚也可能增加拉帕替尼浓度而应避免。如患者必须与强CYP3A4 抑制剂共同给药,根据药代动力学研究。 减低拉帕替尼剂量至500 mg/天预计调整拉帕替尼AUC至无抑制剂观察到范围而应被考虑吧。但是,在接受强CYP3A4抑制剂患者没有这种调整剂量的临床资料。如强抑制剂被终 止,拉帕替尼剂量是向上调整至适应证剂量前应允许有约1周清洗期[见药物相互作用(7.2).]。
同时强CYP3A4诱导剂:应避 免同时使用强CYP3A4诱导剂 (如, 地塞米松[dexamethasone], 苯妥英[phenytoin], 卡马西平[carbamazepine],利福平[rifampin],利福布丁[rifabutin],利福喷丁[rifapentin],苯巴比妥 [Phenobarbital],圣约翰草[St. John’s Wort])。如患者必须与强CYP3A4诱导剂共同给药,根据药代动力学研究,拉帕替尼的剂量应根据耐受性逐步递增从1,250 mg/天至4,500 mg/天(HER2阳性转移乳腺癌适应证)或从1,500 mg/天递增至5,500 mg/天(激素受体阳性,HER2阳性乳腺癌适应证)。应考虑拉帕替尼的剂量预计调整拉帕替尼AUC至无诱导剂观察到范围。但是,没有患者接受强 CYP3A4诱导剂用这种调整剂量临床资料。如强诱导剂被终止,拉帕替尼剂量应减低至适应剂量[见药物相互作用 (7.2).]。
其它毒性:当患者发生2级NCI CTCAE毒性可考虑终止或中断泰克布给药和当毒性改善至1级或更低可在1,250 mg/天重新开始。如毒性再发生,那么泰克布与卡培他滨联用应在较低剂量再开始(1,000 mg/天)和来曲唑联用 应在较低剂量1,250 mg/天再开始。
为共同给药产品见有关制造商的处方资料的剂量调整指导原则在毒性事件和其它相关安全性资料或禁忌证。
3 剂型和规格
250 mg片— 椭圆形,双凸面,橙色,和一侧凹入GS XJG图案的薄膜包衣片。
4 禁忌证
在有已知对本品或其任何组分严重超敏性(如,过敏反应)患者中禁忌泰克布。
5 警告和注意事项
5.1 左心室射血分数减低
曾报道泰克布减低LVEF[见不良反应(6.1)]。在临床试验中,大多数(>57%) LVEF减低发生在治疗的头12周内;但是,对长期暴露数据有限。如泰克布是被给予至可能损伤左心室功能情况的患者应谨慎对待。所有患者开始用泰克布治疗 前应评价LVEF确保患者基线LVEF是在该机构正常限度以内。用泰克布治疗期间应继续评价LVEF以保证LVEF没有下降至机构正常低限以下[见剂量和 给药方法(2.2)]。
5.2 肝毒性
在临床试验(<1%患者)和上市后经验中曾观察到肝毒性(ALT或AST>正常上限3倍和总胆红素>正常上限2倍)。曾报道肝毒性可能 严重和死亡。未确定死亡的因果关系。肝毒性可能发生在治疗开始后几天至几月。治疗开始前,治疗期间每4至6周,和当临床指示时应监测肝功能试验(转氨酶, 胆红素,和碱性磷酸酶)。如肝功能变化严重,应终止用泰克布治疗而患者不应用泰克布再次治疗[见不良反应(6.1)]。
5.3 有严重肝受损患者
如泰克布是将给予有严重预先存在肝受损患者时, 应考虑减低剂量。[见剂量和给药方法(2.2)和在特殊人群中使用(8.7)]。当治疗时发生严重肝毒性患者,应终止泰克布而患者不应用泰克布再次治疗[见警告和注意事项(5.2)]。
5.4 腹泻
用泰克布治疗期间曾报道腹泻,包括严重腹泻 [见不良反应(6.1)]。腹泻用抗-腹泻药的主动处理很重要。严重腹泻病例可能需要口服或静脉给予电解质和液体,以及中断或终止用泰克布治疗。
5.5 间质性肺疾病/肺炎
在单药治疗或与其它化疗联用时,拉帕替尼曾伴随间质性肺疾病和肺炎[见不良反应(6.1)]。应监查患者指示间质性肺疾病或肺炎的肺症状。患者经受指示间质性肺疾病/肺炎为3级(NCI CTCAE)肺症状时应终止泰克布。
5.6 QT延长
在晚期癌症患者中的一项拉帕替尼非对照,开放剂量递增研究中观察到QT延长[见临床药理学(12.4)]。对已经或可能发生QTc延长患者应谨慎给予拉帕 替尼。这些情况还包括有低钾血症或低镁血症,有先天性长QT综合征患者,用抗-心律失常药物或其它导致QT延长的药品,和累积高剂量蒽环类药物治疗的患 者。拉帕替尼给药前应纠正低钾血症或低镁血症。
5.7 妊娠中使用
当给予妊娠妇女泰克布可致胎儿危害。根据动物中的发现,泰克布预期导致不良生殖效应。在器官形成和至哺乳期时给予大鼠拉帕替尼导致出生后头4天内子代死亡 [见在特殊人群中使用(8.1)]。在妊娠妇女中没有用泰克布适当和对照良好的研究。建议服用泰克布妇女不要成为妊娠。如妊娠时使用此药,或如服用药物时 患者成为妊娠,应忠告患者对胎儿潜在的危害。
6 不良反应
6.1 临床试验经验
因为临床试验是在广泛不同条件性进行,在某药临床试验中观察到不良反应率不能直接与另一药物临床试验发生率直接比较而且可能不反映实践中观察到的发生率。
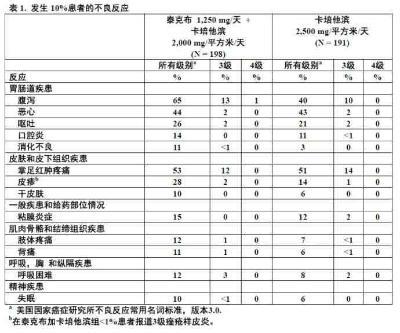
HER2阳性转移乳腺癌:在临床试验中曾在12,000以上患者评价泰克布的安全性。在一项随机化,3期试验在198例患者中评价泰克布与卡培他滨联用在 乳腺癌的疗效和安全性。[见临床研究(14.1).]。表1中显示任何治疗组发生至少10%患者或联用治疗组较高的不良反应。
用泰克布加卡培他滨治疗期间最常见不良反应(>20%)是胃肠道(腹泻,恶心,和呕吐),皮肤学(掌足红肿疼痛和皮疹),和疲劳。腹泻是导致研究药物终止的最常见不良反应。
最常见3和4级不良反应(NCI CTCAE v3)是腹泻和掌足红肿疼痛. 在表2中显示选定的实验室异常。
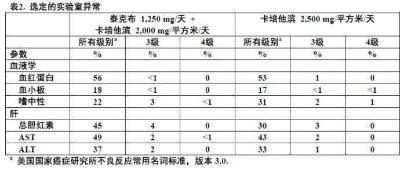
激素受体阳性,转移乳腺癌:在一项随机化临床试验有激素受体阳性,转移乳腺癌患者(N = 1,286),对其转移疾病未曾接受过
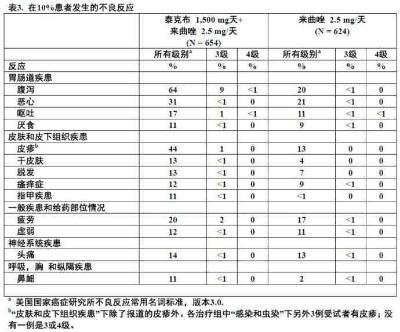
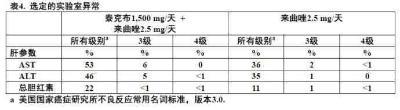
化疗,患者接受来曲唑有或无泰克布。在这项试验中,泰克布的安全性谱形是与来自泰克布在晚期或转移乳腺癌人群试验既 往报道的结果一致。表3中显示在任何治疗组发生至少10%患者和联合治疗组较高的不良反应。表4中显示选定的实验室异常。
左心室射血分数减低:由于潜在心脏毒性用HER2(ErbB2)抑制剂,临床试验中在约8-周间隔监视LVEF。LVEF 减低被定义为当左心室心脏功能体征和症状的恶化是3级(NCI CTCAE),或左心室心脏射血分数相对于基线减低20%,是低于机构的正常低限。在198例接受泰克布/卡培他滨联用治疗患者中,3例经受2级和1例有 3级LVEF不良反应(NCI CTCAE v3)。[见警告和注意事项(5.1).]。654例接受泰克布/来曲唑联用治疗患者中,26例患者经受1或2级和6例患者有3或4 级LVEF不良反应。
肝毒性:泰克布曾伴随肝毒性[见黑框警告和警告和注意事项(5.2)]。
间质性肺疾病/肺炎:泰克布单药治疗或与其它化疗联用曾伴随间质性肺疾病和肺炎[见警告和注意事项(5.5)]。
6.2 上市后经验
批准后使用泰克布期间曾鉴定以下不良反应。因为这些反应是从人群大小不确定志愿报告的,并非总可能可靠估计其频数或确定与药物暴露因果相互关系。
免疫疾患:超敏性反应包括过敏反应[见禁忌证(4)]。
皮肤和皮下组织疾患:指甲疾患包括甲沟炎。
7 药物相互作用
7.1 拉帕替尼对药物代谢酶和药物转运系统的影响
拉帕替尼在体外在临床有意义浓度抑制CYP3A4和CYP2C8。当拉帕替尼与治疗窗狭窄的CYP3A4或CYP2C8底物的药物同时给药时应小心对待和 应考虑减低同时给予底物药物的剂量。在体外人肝微粒体中拉帕替尼不显著抑制以下酶: CYP1A2,CYP2C9,CYP2C19,和CYP2D6或UGT酶,但是,不知道其临床意义。
拉帕替尼抑制人P-糖蛋白。如泰克布与P-gp底物药物给药时,很可能增加底物药物浓度,而应小心对待。
紫杉醇:在癌症患者接受泰克布和CYP2C8底物紫杉醇,紫杉醇的24-小时全身暴露(AUC)增加23%。由于研究设计缺陷,这个来自体内评价的紫杉醇暴露的增加可能被低估。
7.2 抑制或诱导细胞色素P450 3A4酶药物
拉帕替尼被CYP3A4进行广泛代谢,而同时给予CYP3A4的强抑制剂或诱导剂显著改变拉帕替尼浓度(见下文酮康唑和卡马西平节)。对必须同时接受CYP3A4酶强抑制剂或同时强诱导剂患者应考虑调整拉帕替尼的剂量[见剂量和给药方法(2.2)]。
酮康唑:在健康受试者中接受酮康唑,一种CYP3A4抑制剂,在200 mg每天2次共7天,全身暴露(AUC)至拉帕替尼被增加至约对照的3.6-倍和半衰期增加至对照的1.7-倍。
卡马西平:在健康受试者中接受the CYP3A4诱导剂,卡马西平,剂量100 mg每天2次共3天和200 mg每天2次共17天,对拉帕替尼全身暴露(AUC)减低约72%。
7.3 抑制药物转运系统药物
拉帕替尼是流出转运蛋白 P-糖蛋白(P-gp, ABCB1)的底物。如泰克布与抑制P-gp药物给药,很可能增加拉帕替尼浓度,和应谨慎对待。
8 在特殊人群中使用
8.1 妊娠
妊娠类别D[见警告和注意事项(5.7)].
根据动物中的发现,当给予妊娠妇女泰克布可能致胎儿危害。在器官形成期和至哺乳时给予大鼠拉帕替尼导致生下后头4天内子代死亡。当器官形成期时给予妊娠动 物母体毒性剂量,拉帕替尼引起胎畜异常(大鼠)或流产(兔)。在妊娠妇女中没有用泰克布适当和对照良好的研究。建议服用泰克布妇女不要成为妊娠。如妊娠期 间使用此药,或服药时患者成为妊娠,应忠告患者对胎儿潜在危害。
在一项 研究 妊娠大鼠在器官形成期至哺乳给予拉帕替尼,在剂量120 mg/kg/天( 根据AUC为人临床暴露 拉帕替尼加卡培他滨 1,250 mg剂量后约6.4倍 ), 91%幼畜在出生后第4天死亡。而34% 60 mg/kg/天 幼畜死亡 。在本研究中最高无效应剂量是20 mg/kg/天 (根据AUC约等于人临床暴露 )。
在妊娠大鼠和兔给予口服剂量30, 60,和120 mg/kg/天. 研究拉帕替尼 对胚胎胎儿发育的影响。没有 致畸胎效应; 但是, 在母体毒性剂量120 mg/kg/天 (根据AUC拉帕替尼加卡培他滨1,250 mg 计量后人临床暴露的约6.4倍),出现次要异常 (左侧脐动脉,颈肋和早熟骨化) 。在兔中,拉帕替尼在 60和120 mg/kg/天 伴随母体毒性(根据AUC 拉帕替尼加卡培他滨1,250 mg剂量后人临床暴露分别约0.07和0.2倍)和流产在120 mg/kg/天.母体毒性是伴随胎儿体重减低和次要骨骼变异。
8.3 哺乳母亲
不知道拉帕替尼是否排泄至人乳汁。因为许多药物排泄至人乳汁和因为哺乳婴儿来自泰克布的潜在严重不良反应,应做出决策是否终止哺乳或终止药物,考虑药物对母亲的重要性。
8.4 儿童使用
尚未在儿童患者中确定泰克布的安全性和有效性。
8.5 老年人使用
在泰克布与卡培他滨联用(N = 198)临床研究中转移乳腺癌患者总数中,17%是65岁和以上,和1%是75岁和以上。在泰克布与来曲唑联用临床研究激素受体阳性,HER2阳性转移乳 腺癌患者总数(N = 642)中,44%是65岁和以上,和12%是75岁和以上。年老受试者和较年轻受试者间未观察到安全性和有效性中总体差别,而其它报道的临床经验未确定 老年和较年轻患者间反应的差别,但不能除外某些老年个体灵敏度更低的可能性。
8.6 肾受损
未曾在肾受损患者或正在进行血液透析患者中进行专门的拉帕替尼药代动力学研究。没有在有严重肾受损患者中用泰克布的经验。但是,因小于2% (拉帕替尼和其代谢物)给药剂量被肾消除,肾受损很可能不影响拉帕替尼的药代动力学。
8.7 肝受损
在预先存在中度(n = 8)或严重(n = 4)肝受损受试者(分别Child-Pugh Class B/C)和在8例健康对照受试者中检查拉帕替尼的药代动力学。预先存在中度和严重肝受损受试者中单次口服100-mg剂量后对拉帕替尼全身暴露(AUC) 分别约增加14%和63%。由于对药物暴露增加有严重肝受损患者中给予泰克布应谨慎对待。对预先存在严重肝受损患者应考虑减低剂量[见剂量和给药方法 (2.2)]。当治疗时发生严重肝毒性患者,应终止泰克布而且患者不应用泰克布再次治疗[见警告和注意事项(5.2)]。
10 药物过量
对泰克布过量无已知解毒剂。在临床试验中拉帕替尼曾被给予最大口服剂量是1,800 mg每天1次。更频摄入泰克布可能导致血清浓度超出在临床试验中观察到和可能导致增加毒性。所以,丢失剂量不应替代和给药应恢复下一次计划的每天剂量。
曾有一篇报道一例患者服3,000 mg泰克布工10天,这例患者在第10天有3级腹泻和呕吐。静脉水化后和中断用泰克布和来曲唑治疗后事件解决。
因为拉帕替尼在肾无显著排泄和它与血浆蛋白高度结合, 血液透析预期不是增强拉帕替尼消除的有效方法。
11 一般描述
拉帕替尼[Lapatinib]是一种小分子和4-苯基氨基喹唑啉类激酶抑制剂的成员。存在为二苯磺酸盐的一水化物,有化学名N-(3-chloro- 4-{[(3-fluorophenyl)methyl]oxy}phenyl)-6-[5-({[2-(methylsulfonyl)ethyl]amino}methyl)- 2-furanyl] -4-quinazolinamine bis(4-methylbenzenesulfonate) 一水化物。其分子式C29H26ClFN4O4S(C7H8O3S)2 H2O和分子量943.5。拉帕替尼二苯磺酸盐一水化物有下列化学结构式:
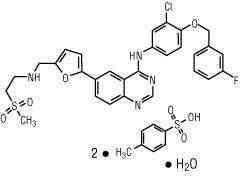
拉帕替尼是抑制黄色固体,和在25℃在水中溶解度为0.007 mg/mL和在 0.1N HCl为0.001 mg/mL。
泰克布的各250 mg片含405 mg拉帕替尼二苯磺酸一水化物,等同于398 mg拉帕替尼二苯磺酸或250 mg拉帕替尼游离碱。
泰克布的无活性成分是:片核心:硬脂酸镁,微晶纤维素,聚乙烯吡啶酮,羟基乙酸淀粉钠。涂层:橙色薄膜衣:FD&C黄色6号/日落黄FCF铝色淀,羟丙甲纤维素,聚乙二醇/PEG 400,聚山梨醇80,二氧化钛。
12 临床药理学
12.1 作用机制
拉帕替尼是表皮生长因子受体(EGFR[ErbB1])和人表皮受体型2(HER2[ErbB2])受体两者细胞内酪氨酸激酶结构区的一种4-苯基氨基喹 唑啉激酶抑制剂(Ki app估计值分别为3nM和13nM)有一个解离半衰期300分钟。拉帕替尼在体外和在各种动物模型中抑制ErbB-驱动肿瘤细胞生长。
在一项体外研究中当拉帕替尼和5-FU(卡培他滨的活性代谢物)在4种受试的肿瘤细胞株中被联合使用显示相加作用。在曲妥珠单抗-条件细胞株中评价拉帕替 尼的抑制生长效应。在体外长期生长在含曲妥珠单抗介质中选择的乳腺癌细胞株拉帕替尼保留明显活性。这些体外发现提示这两种药物间无交叉耐药性。
激素受体阳性乳腺癌细胞(有ER[雌激素受体]和/或PgR[孕激素受体])共表达HER2趋向于对确定的内分泌治疗耐药。相似地,激素受体阳性乳腺癌细胞最初缺乏EGFR或HER2当肿瘤成为对内分泌治疗耐药时,上调这些受体蛋白。
12.3 药代动力学
吸收:口服给予泰克布后吸收是不完全和变异的。在中位滞后时间0.25小时后出现血清浓度(范围0至1.5小时)。给药后约4小时达到拉帕替尼的血浆峰浓度(Cmax)。泰克布的每天给药在6至7天内达到稳态,表明有效半衰期24小时。
在每天剂量1,250 mg,稳态几何Cmax均数值(95%可信区间)为2.43 μg/mL(1.57至3.77 μg/mL)和AUC为36.2 μg/hr/mL (23.4至56 μg/hr/mL)。
泰克布每天剂量分次给药与相同总量给予每天1次比较导致在稳态(稳态AUC) 暴露约较高2-倍。
当与食物给药市拉帕替尼全身暴露增加。拉帕替尼AUC值是当与低脂肪给药(5% 脂肪-500卡)或与高脂肪 (50%脂肪-1,000卡)餐,分别约3-和4-倍较高(Cmax约较高2.5-和3-倍)。
分布:拉帕替尼与白蛋和α-1酸性糖蛋白白高度结合(>99%)。在体外研究表明拉帕替尼是对转运蛋白乳腺癌耐药蛋白(BCRP,ABCG2)和 P-糖蛋白(P-gp, ABCB1)的底物。在体外曾显示在有临床意义浓度拉帕替尼抑制这些流出转运蛋白,以及肝摄取转运蛋白OATP 1B1。
代谢:拉帕替尼进行广泛代谢,主要被CYP3A4和CYP3A5,次要贡献来自CYP2C19和CYP2C8生成各种氧化代谢物,在粪中回收没有一个占超过剂量14%或血浆拉帕替尼浓度的10%。
消除:在临床剂量,单次剂量后末端半衰期为14.2小时;重复给药表明积蓄有效半衰期24小时。
拉帕替尼的消除主要通过CYP3A4/5代谢与忽略的(<2%)肾排泄。在粪中回收母体拉帕替尼占口服剂量中位27%(范围3至67%)。
年龄,性别,或种族的影响:未曾进行年龄,性别,或种族对拉帕替尼的药代动力学影响的研究。
12.4 QT延长
作为一项晚期癌症患者非对照开放剂量递增研究的一部分评估拉帕替尼延长QT的潜能。81例患者接受每天剂量拉帕替尼范围从175 mg/天至1,800 mg/天。在第1天和第14天系列采集ECGs评价拉帕替尼QT间期的影响。资料分析提示恒定的浓度依赖性QTc间隔的延长。
13 非临床毒理学
13.1 癌发生, 突变发生, 生育力受损
正在用拉帕替尼进行2年致癌性研究。
在中国仓鼠卵巢染色体畸变分析,微生物突变发生(Ames)分析,人淋巴细胞染色体畸变分析或体内在单剂量直至2,000 mg/kg大鼠骨髓染色体畸变分析中,拉帕替尼不是致染色体断裂的或突变发生的。但是,在药物产品的一个杂质(达4 ppm或8 mμ/天)当在体外和体内二种分析中单独试验是遗传毒性。
在雌性中剂量达120 mg/kg/天和在雄性中180 mg/kg/天(根据AUC1,250 mg剂量的拉帕替尼加卡培他滨后期望人临床暴露分别约6.4倍和2.6倍) 对雄性或雌性大鼠交配或生育力没有影响。拉帕替尼对人生育力影响不知道。但是,当雌性大鼠生育期和至怀孕头6天被给予口服剂量拉帕替尼20 mg/kg/天,见到显著减少活胎鼠数和在60 mg/kg/天时减低胎鼠体重(根据AUC分别拉帕替尼加卡培他滨1,250 mg剂量人预期临床暴露的约6.4倍和3.3 倍)。
14 临床研究
14.1 HER2阳性转移乳腺癌
在一项随机化,3期试验中评价泰克布与卡培他滨联用在乳腺癌中的疗效和安全性。为合格纳入患者有HER2(ErbB2)过表达(用FISH证实的IHC 3+或IHC 2+),局部晚期或转移乳腺癌,包括蒽环类药物,紫杉烷,和曲妥珠单抗既往治疗后进展。
患者被随机化接受或泰克布1,250 mg每天1次(连续地)加卡培他滨2,000 mg/平方米/天每21天在第1-14天,或接受单独卡培他滨在剂量2,500 mg/平方米/天每21天在第1-14天。终点是至进展时间(TTP)。TTP的定义是从随机化至肿瘤进展或乳腺癌相关死亡的时间。根据预先指定中期分析 的结果,终止进一步纳入。本研究纳入399例患者。中位年龄是53岁和14%是大于65岁。91%是高加索人。97%有IV期乳腺癌。48%为雌激素受 体+(ER+)或孕激素受体+(PR+),和95%是用FISH证实ErbB2 IHC 3+或IHC 2+。约95%患者有用蒽环类药物,紫杉烷,和曲妥珠单抗既往治疗。
在表5,图1,和图2中展示4个月后疗效分析。
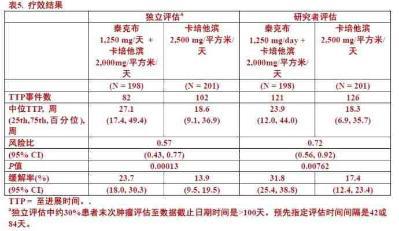
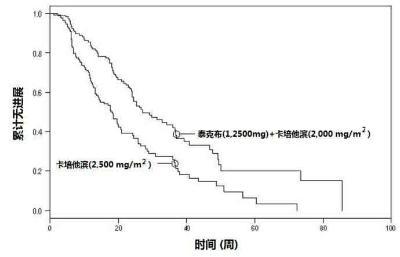
图1.独立评审委员会-评价至进展时间的Kaplan-Meier估计值
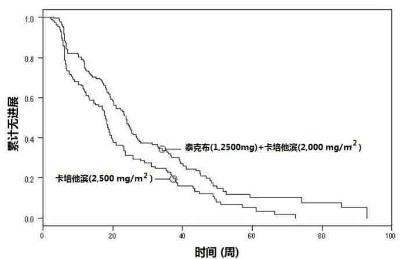
图2.研究者评估至进展时间的Kaplan-Meier估计值
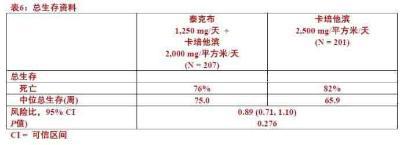
以上疗效分析时,总生存数据不够成熟(32%事件)。但是,根据TTP结果,研究被解盲态而单独接受卡培他滨患者被允许交叉至泰克布加卡培他滨治疗。生存数据被跟踪另外2年而数据成熟和在表6中总结分析。
14.2 激素受体阳性,HER2阳性转移乳腺癌
在一项双盲,安慰剂对照,多中心研究中评价泰克布与来曲唑联用的疗效和安全性。总共1,286例有激素受体阳性(ER阳性和/或PgR阳性)转移乳腺癌绝 经后妇女,对转移病未曾接受既往治疗,被随机赋予接受或泰克布(1,500 mg每天1次)加来曲唑(2.5 mg每天1次)(n = 642)或单独来曲唑(2.5 mg每天1次)(n = 644)。所有随机化至治疗患者中219例(17%)患者有肿瘤过表达HER2受体,定义为萤光原位杂交(FISH)2或免疫组化(IHC)3+。有 952例(74%)患者为HER2阴性和115例(9%)患者没有被证实的HER2受体状态。主要目的是在HER2阳性人群中评价和比较无进展生存 (PFS)。无进展生存被定义为随机化日期和首次记录由于任何原因疾病进展或死亡征象的最早日期间的时间间隔。
两治疗组间基线人口统计指标和疾病特征被平衡。中位年龄为63岁和45%是65岁或以上。84%患者为白种人。约50% HER2阳性人群有既往辅助/新辅助化疗和56%有既往激素治疗。只有2例患者有既往曲妥珠单抗。
在HER2阳性子组(n = 219),泰克布添加至来曲唑导致PFS改善。在HER2阴性子组,泰克布加来曲唑联用与单独来曲唑加安慰剂比较PFS无改善。用泰克布加来曲唑联合治疗 总缓解率(ORR)也改善。总生存(OS)数据未成熟。表7和图3中展示激素受体阳性,HER2阳性和HER2阴性子组的疗效分析。
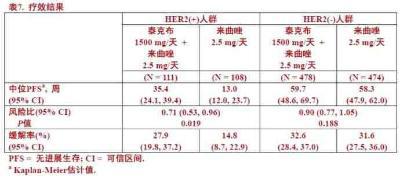
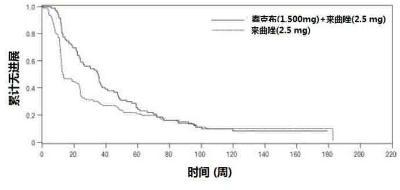
图3.对HER2阳性人群无进展生存的Kaplan-Meier估计值。
16 如何供应/贮存和处置
泰克布250 mg片是椭圆形,双凸面,橙色,和一侧凹入GS XJG图案的薄膜包衣片和可得到:
瓶内150片:NDC 0173-0752-00
贮藏在25℃ (77℉);外出允许至15至30℃ (59至86℉) [见美国药典控制室温]。

